„Mercaptopurin“ – Versionsunterschied
| [gesichtete Version] | [gesichtete Version] |
Rjh (Diskussion | Beiträge) +GHS | JWBE (Diskussion | Beiträge) Formalia | ||
| Zeile 16: | Zeile 16: | ||
| pKs = | | pKs = | ||
| Dichte = | | Dichte = | ||
| Schmelzpunkt = 140 °C | | Schmelzpunkt = 140 [[Grad Celsius|°C]]<ref name="GESTIS"/> | ||
| Siedepunkt = 313–314 °C <small>Zersetzung</small> | | Siedepunkt = 313–314 °C <small>Zersetzung</small><ref name="GESTIS"/> | ||
| Dampfdruck = | | Dampfdruck = | ||
| Löslichkeit = | | Löslichkeit = | ||
| Quelle GHS-Kz = <ref name="Sigma">{{Sigma-Aldrich|ALDRICH|852678|Datum=9. April 2011|Name=6-Mercaptopurine monohydrate}}</ref> | | Quelle GHS-Kz = <ref name="Sigma">{{Sigma-Aldrich|ALDRICH|852678|Datum=9. April 2011|Name=6-Mercaptopurine monohydrate}}</ref> | ||
| GHS-Piktogramme = {{GHS-Piktogramme|07}} | | GHS-Piktogramme = {{GHS-Piktogramme|07}} | ||
| GHS-Signalwort = Achtung | | GHS-Signalwort = Achtung | ||
| H = {{H-Sätze|302|315|319|335}} | | H = {{H-Sätze|302|315|319|335}} | ||
| EUH = {{EUH-Sätze|-}} | | EUH = {{EUH-Sätze|-}} | ||
| P = {{P-Sätze|261|305+351+338}} | | P = {{P-Sätze|261|305+351+338}} | ||
| Quelle P = <ref name="Sigma" /> | | Quelle P = <ref name="Sigma" /> | ||
| Quelle GefStKz = <ref name=" | | Quelle GefStKz = <ref name="GESTIS">{{GESTIS|Name=6-Mercaptopurin|ZVG=100021|CAS=50-44-2|Datum=23. Mai 2009}}.</ref> | ||
| Gefahrensymbole = {{Gefahrensymbole-klein|Xn}} | | Gefahrensymbole = {{Gefahrensymbole-klein|Xn}} | ||
| R = {{R-Sätze|22|36/37/38|62|63}} | | R = {{R-Sätze|22|36/37/38|62|63}} | ||
| Zeile 45: | Zeile 45: | ||
== Pharmakogenetik == | == Pharmakogenetik == | ||
Mercaptopurin wird durch das Enzym [[Thiopurin-Methyltransferase]] (TPMT) metabolisiert. Dieses Enzym zeigt einen relevanten [[Polymorphismus]] in der menschlichen Bevölkerung. Etwa 10 % der Bevölkerung weisen eine deutlich verminderte Enzymaktivität auf und etwa 0,3 % (d. h. einer unter 300) zeigen gar keine nachweisbare TPMT-Aktivität. Bei diesen Patienten kann es zu unerwartet hohen Toxizitäten kommen, wenn Mercaptopurin in „normaler“ Dosis verabreicht wird. Besonders betroffen ist die Blutbildung, wo es zu einer ausgeprägten [[Zytopenie]] ([[Leukopenie]], [[Anämie]], [[Thrombopenie]]) kommen kann. Ursache der verminderten oder fehlenden Enzymaktivität sind Mutationen im [[Gen]] für TPMT. Drei [[Allel]]e (TPMT *2, *3A und *3C), sind für etwa 80–95 % der Fälle von verminderter TPMT-Aktivität verantwortlich.<ref>Zhou S. ''Clinical pharmacogenomics of thiopurine S-methyltransferase | Mercaptopurin wird durch das Enzym [[Thiopurin-Methyltransferase]] (TPMT) metabolisiert. Dieses Enzym zeigt einen relevanten [[Polymorphismus]] in der menschlichen Bevölkerung. Etwa 10 % der Bevölkerung weisen eine deutlich verminderte Enzymaktivität auf und etwa 0,3 % (d. h. einer unter 300) zeigen gar keine nachweisbare TPMT-Aktivität. Bei diesen Patienten kann es zu unerwartet hohen Toxizitäten kommen, wenn Mercaptopurin in „normaler“ Dosis verabreicht wird. Besonders betroffen ist die Blutbildung, wo es zu einer ausgeprägten [[Zytopenie]] ([[Leukopenie]], [[Anämie]], [[Thrombopenie]]) kommen kann. Ursache der verminderten oder fehlenden Enzymaktivität sind Mutationen im [[Gen]] für TPMT. Drei [[Allel]]e (TPMT *2, *3A und *3C), sind für etwa 80–95 % der Fälle von verminderter TPMT-Aktivität verantwortlich.<ref>Zhou S. ''Clinical pharmacogenomics of thiopurine S-methyltransferase'', in: ''[[Curr. Clin. Pharmacol.]]'', '''2006''', ''1'' (1), S. 119–128; PMID 18666383.</ref> Diagnostisch wird die TPMT-Aktivität meist in den [[Erythrozyt]]en bestimmt, so dass diese Untersuchung durchgeführt werden sollte, bevor der Patient [[Bluttransfusion]]en erhalten hat, da dann die Enzymaktivität falsch normal sein kann. | ||
== Siehe auch == | == Siehe auch == | ||
| Zeile 52: | Zeile 52: | ||
== Einzelnachweise == | == Einzelnachweise == | ||
<references/> | <references/> | ||
{{Gesundheitshinweis}} | {{Gesundheitshinweis}} | ||
{{SORTIERUNG:Mercaptopurin6}} | |||
[[Kategorie:Purin]] | [[Kategorie:Purin]] | ||
[[Kategorie:Nucleinbase]] | [[Kategorie:Nucleinbase]] | ||
Version vom 9. April 2011, 09:28 Uhr
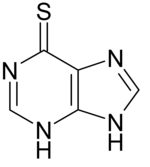
| Strukturformel | |||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
 | |||||||||||||
| Allgemeines | |||||||||||||
| Freiname | Mercaptopurin | ||||||||||||
| Andere Namen | 7H-Purin-6-thiol | ||||||||||||
| Summenformel | C5H4N4S | ||||||||||||
| Externe Identifikatoren/Datenbanken | |||||||||||||
| |||||||||||||
| Arzneistoffangaben | |||||||||||||
| ATC-Code | |||||||||||||
| Wirkstoffklasse | |||||||||||||
| Eigenschaften | |||||||||||||
| Molare Masse | 152,18 g·mol−1 | ||||||||||||
| Schmelzpunkt | |||||||||||||
| Siedepunkt | 313–314 °C Zersetzung[1] | ||||||||||||
| Sicherheitshinweise | |||||||||||||
| |||||||||||||
| Soweit möglich und gebräuchlich, werden SI-Einheiten verwendet. Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen (0 °C, 1000 hPa). | |||||||||||||
Mercaptopurin (INN), auch 6-Mercaptopurin, ist ein Analogon der Nukleinbasen Adenin und Guanin. Es wird als Zytostatikum in der Chemotherapie der Leukämie, sowie zur Langzeittherapie chronischer Darmentzündungen eingesetzt. Es wird von GlaxoSmithKline unter dem Handelsnamen Puri Nethol® europaweit vertrieben.
Pharmakologie
Es ist ein Antimetabolit, das heißt es wird bei der Zellteilung anstelle der Purinbasen Adenin und Guanin in die DNA eingebaut. Die entstehende DNA verliert dadurch ihre Funktion.
6-Mercaptopurin entsteht aus dem Prodrug Azathioprin durch Verstoffwechselung in der Leber. Gleichzeitig kann die Wirkung des 6-Mercaptopurins gesteigert werden, indem sein Abbau durch das Urikostatikum Allopurinol gehemmt wird. Dadurch können niedrigere Dosierungen angewandt werden, die weniger unerwünschte Nebenwirkungen hervorrufen.
Bei Unverträglichkeit von Azathioprin wird Mercaptopurin oft vertragen. Während in Deutschland zur Behandlung chronischer Darmentzündungen zunächst Azathioprin eingesetzt wird, beginnt man zum Beispiel in den USA fast ausschließlich mit Mercaptopurin.
Pharmakogenetik
Mercaptopurin wird durch das Enzym Thiopurin-Methyltransferase (TPMT) metabolisiert. Dieses Enzym zeigt einen relevanten Polymorphismus in der menschlichen Bevölkerung. Etwa 10 % der Bevölkerung weisen eine deutlich verminderte Enzymaktivität auf und etwa 0,3 % (d. h. einer unter 300) zeigen gar keine nachweisbare TPMT-Aktivität. Bei diesen Patienten kann es zu unerwartet hohen Toxizitäten kommen, wenn Mercaptopurin in „normaler“ Dosis verabreicht wird. Besonders betroffen ist die Blutbildung, wo es zu einer ausgeprägten Zytopenie (Leukopenie, Anämie, Thrombopenie) kommen kann. Ursache der verminderten oder fehlenden Enzymaktivität sind Mutationen im Gen für TPMT. Drei Allele (TPMT *2, *3A und *3C), sind für etwa 80–95 % der Fälle von verminderter TPMT-Aktivität verantwortlich.[3] Diagnostisch wird die TPMT-Aktivität meist in den Erythrozyten bestimmt, so dass diese Untersuchung durchgeführt werden sollte, bevor der Patient Bluttransfusionen erhalten hat, da dann die Enzymaktivität falsch normal sein kann.
Siehe auch
- Azathioprin, Prodrug von 6-Mercaptopurin
Einzelnachweise
- ↑ a b c Eintrag zu 6-Mercaptopurin in der GESTIS-Stoffdatenbank des IFA (JavaScript erforderlich).
- ↑ a b Datenblatt 6-Mercaptopurine monohydrate bei Sigma-Aldrich (PDF).
- ↑ Zhou S. Clinical pharmacogenomics of thiopurine S-methyltransferase, in: Curr. Clin. Pharmacol., 2006, 1 (1), S. 119–128; PMID 18666383.





