Influenza-A-Virus H5N1
| Influenza A/H5N1 | ||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|
 | ||||||||||||
| Vorlage:Taxonomy | ||||||||||||
| ||||||||||||
| Wissenschaftlicher Name | ||||||||||||
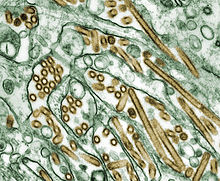
| Influenzavirus typ A/H5N1 | ||||||||||||
A/H5N1 ist die wissenschaftliche Bezeichnung für den Erreger des aktuellen Ausbruchs der so genannten Vogelgrippe. Diese Variante des Erregers ist ein als hoch pathogenes aviäres Influenzavirus (HPAIV) bezeichnetes Influenza-Virus (also ein von Vögeln stammendes Grippevirus) und damit ein behülltes Einzel(-)-Strang-RNA-Virus [ss(-)RNA] aus der Familie der Orthomyxoviren. Diese zunächst in China aufgetretene Variante (der so genannte Asia-Typ) gilt als besonders virulent und ist mehrfach auch auf den Menschen übergegangen. In der zunächst minder pathogenen Form ist das Virus bereits seit 1959 bekannt [1]. Informationen über weitere Influenza-Viren, die ebenfalls unter Geflügel verbreitet sind, siehe unter Geflügelpest.
Besondere Merkmale
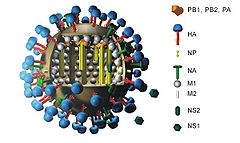
Wie bei allen anderen Influenzaviren auch, kodieren die Segmente dieses Subtyps zehn virale Proteine: Hämagglutinin (HA), Neuraminidase (NA), Nukleoprotein (NP), die Matrixproteine (M1) und (M2), die Polymerase Proteine (PB1), (PB2) und (PA) und die Nichtstrukturproteine (NS1) und (NS2). Eines der acht Gensegmente enthält allein das NS-Gen, welches die beiden Nichtstrukturproteine (NS1) und (NS2) bildet.

Ein Forscherteam um Clayton Naeve vom St. Jude Children's Hospital in Memphis, Tennessee hat durch vergleichende Analysen der RNA von Influenzaviren festgestellt, dass sich an einem Ende des NS-Gens ein Abschnitt befindet, der vermutlich mit über die Heftigkeit eines Infektionsverlaufs entscheidet. Änderungen in diesem Genabschnitt führen zu einer Variation in einem variablen Bereich auf dem NS1-Protein. Bei A/H5N1 besitzt dieser variable Proteinbereich eine Struktur, die sich besonders beim Menschen sehr effektiv an sogenannte PDZ-Domänen (spezieller Teilbereich von Eiweißmolekülen in Zellen) bindet und dadurch die Signalübermittlung in den Zellen besonders stark stört. Eine derartige Störung der Signalübermittlung bewirkt dann eine Überstimulation des Immunsystems, bei der viele Entzündungsbotenstoffe ausgeschüttet werden.
Der hiermit angesprochene Genomabschnitt ist demzufolge auch als einer der Orte anzusehen, bei denen eine Anpassung der verschiedenen Gattungen und Subtypen des Influenza-Virus an ihre jeweiligen Reservoirwirte stattfindet oder schon stattgefunden hat.
In einer Studie, die Mitte März 2006 in der Fachzeitschrift Nature veröffentlicht wurde, [2] argumentierten Forscher, dass sich A/H5N1 im Gegensatz zu den humenen Influenzaviren an Rezeptoren binde, welche sich bei Mensch und Tier vor allem in den Lungenbläschen befinden, aber kaum in den oberen Atemwegen. Dies sei der Grund, dass bisher eine Mensch-zu-Mensch-Übertragung sehr selten auftritt, da eine so genannte Tröpfcheninfektion überwiegend Substanzen aus Hals und Rachen über die Atemluft verbreitet.
Umweltstabilität
Je nach Temperatur ist die Umweltstabilität der Influenzaviren und damit auch des Subtyps A/H5N1 mit all seinen weiteren Varianten sehr unterschiedlich. Bei einer normalen sommerlichen Tagestemperatur von etwa 20° C können an Oberflächen angetrocknete Viren in der Regel zwei bis acht Stunden überdauern. Bei 22° C überstehen sie sowohl in Exkrementen wie auch in Geweben verstorbener Tiere und in Wasser mindestens vier Tage, bei einer Temperatur von 0° C mehr als 30 Tage und im Eis sind sie nahezu unbegrenzt infektionsfähig.
Oberhalb von 22° C verringert sich allerdings die Umweltstabilität auch von A/H5N1 sehr deutlich. Bei 56° C werden die Viren innerhalb von 3 Stunden und bei 60° C innerhalb von 30 Minuten inaktiviert [3]. Ab 70° C sterben sie ab und verlieren damit auch endgültig ihre Infektiösität.
Klassifikation der Subtypen
Bei diesen Influenzaviren gibt es vier Gattungen: Influenza-A, Influenza-B, Influenza-C und das Thogotovirus. Vögel werden nur von Influenza-A-Viren und deren Varianten bzw. Subtypen befallen.
Durch ständige Genveränderungen (Mutationen) entstehen fortwährend neue Varianten der Grippeviren. Diese werden nach bestimmten Oberflächeneigenschaften in Subtypen eingeteilt.
Bisher wurden 16 H-Untertypen und 9 N-Untertypen erkannt. Der Subtyp A/H5N1 etwa hat auf seiner Oberfläche die 5. Variante des Hämagglutinins (H5) sowie die 1. Variante der Neuraminidase (N1). Diese Untertypen befallen üblicherweise jeweils nur bestimmte Wirte, während sie von einer weiteren Anzahl an Infektionsvektoren verbreitet werden können, ohne dass diese Tiere erkranken. Der Subtyp A/H5N1 ist aggressiver als A/H7N7 und SARS.
Mittlerweile sind selbst auch innerhalb des Subtyp A/H5N1 weitere Varianten festgestellt (identifiziert) worden, die sich auch in ihrer ohnehin schon hohen Pathogenität noch deutlich unterscheiden. Besonders die asiatische H5N1-Variante (A/Vietnam/H5N1/1203/2004) ist durch ihre gesteigerte Aggressivität und Pathogenität aufgefallen. Einer Hongkonger Forschergruppe zufolge setzt diese Variante in besonders starken Maße vor allem in der Lunge bestimmte entzündungsfördernde Stoffe (Zytokine, speziell Interleukin 6) frei, die normalerweise ganz allgemein die Immunantwort des Körpers gegen eingedrungene Erreger aktivieren. Diese übermäßige (exzessive) Zytokinfreisetzung führt jedoch zu einer Überreaktion des Immunsystems und damit zu einer Zerstörung vor allem des Lungengewebes und in der Regel rasch zu einem schweren toxischen Schock und zu Multiorganversagen.
Zur genauen Erläuterung der Variabilität der Erreger siehe unter Influenza.
Nachweismethoden
Zum Nachweis von A/H5N1 kommt in der Regel eine abgestufte virologische Diagnostik zum Einsatz.
So stehen Schnelltests zum Nachweis von Influenza-A-Viren zur Verfügung, die auch in der Lage sind, H5N1-Viren zu erkennen. Als Untersuchungsmaterial werden hierfür Nasen- und Rachenabstriche genommen. Erste Ergebnisse liegen dann innerhalb von 20 bis 30 Minuten vor.
Für einen - genaueren - Labornachweis wird zunächst aus einer organischen Probe (bei toten Tieren meist aus Lunge oder Gehirn, bei lebenden Tieren meist aus dem Kot oder von einem Rachenabstrich) mit Hilfe der Polymerase-Kettenreaktion (PCR) das hochkonservative Matrix-Gen (M-Gen) nachzuweisen versucht, das allen Influenza A-Viren eigen ist.
Konnte auf diese Weise eine Infektion mit Influenza A-Viren bestätigt werden, wird die PCR erneut eingesetzt, um mit Hilfe ausgewählter Erkennungssequenzen die Hämagglutinin-Variante 5 (H5) nachzuweisen sowie - parallel dazu - die 1. Variante der Neuraminidase (N1). Sind auch diese beiden Befunde positiv, folgt im dritten Schritt eine genaue Sequenzierung der Erreger-RNA, um darzustellen, ob die minder pathogene oder die hoch pathogene Variante des Erregers vorliegt.
In weniger entwickelten, außereuropäischen Regionen und – als Schnelltest - auch in Europa kommen ferner ältere, erprobte und preiswerte, aber weniger genaue (indirekte serologische) Tests zum Einsatz, so zum Beispiel der Hämagglutinationstest, mit dessen Hilfe eine früher (vor Wochen) überstandene Influenza-Infektion bestätigt werden kann und der Hämagglutinations-Hemmtest, ein Antikörpertest.
Genveränderungen
Der Subtyp A/H5N1 gilt auch aus den schon oben dargestellten Erkenntnissen heute als besonders aggressiv (HPAI, Highly Pathogenic Avian Influenza). Der Virologe Robert G. Webster hebt als besondere Eigenschaft dieses Subtyps hervor, dass er, wie die Variante H7 und anders als alle anderen Subtypen, zuerst die Lunge befällt und sich anschließend im ganzen Körper ausbreitet und bei Vögeln auch Herz, Leber und Gehirn zerstört. Deshalb tötet er heute sehr schnell befallene Vögel, die nicht zu seinem Virusreservoir gehören, und er wird daher von Wissenschaftlern wegen seiner pathogenen Eigenschaften auf Interdependenzen mit anderen Stämmen und Überschreitungen der Artenbarriere aufmerksam beobachtet.
Vor der erwähnten und vor zwei weiteren nachgewiesenen Genveränderungen (die nach Expertenmeinung Ende 1996/Anfang 1997 und 2003 geschahen) war der Erreger bereits mehrfach in Europa aufgetreten, er galt aber als wenig aggressiv. Auch heute noch werden vereinzelt Wildvögel gefunden, die mit dieser minder pathogenen Variante infiziert sind, aber kaum Krankheitssymptome zeigen, so u.a. im Jahr 2004 in Frankreich und Mitte November 2005 bei einer Ente in der Nähe von Padua.
Eine der zunächst 2003 in Hongkong und in Vietnam und dann wieder Anfang 2006 bei den in der Türkei verstorbenen Kindern nachgewiesenen Genveränderungen (bezüglich einer Aminosäure an Position 223 des Hämagglutinin-Rezeptorproteins) erlaubt es den Viren laut einem Bericht in der Nature" [4], sich leichter als zuvor an menschliche Zellen zu binden. Eine zweite, ebenfalls bei den türkischen Kindern nachgewiesene Genveränderung bewirkt den Austausch von Glutaminsäure gegen Lysin in Position 627 seines Polymerase-Proteins, das den Viren dazu dient, ihr genetisches Material zu vervielfältigen. Diese Mutation wurde andernorts gleichfalls schon früher nachgewiesen, allerdings noch nie in Kombination mit der Mutation an Position 223 des Hämagglutinin-Rezeptorproteins. Sie war auch 2003 in den Niederlanden nachgewiesen worden, als dort ein Mann an einer H7N7-Infektion starb und ist eine von insgesamt 10 Mutationen, die dem Virus der Spanischen Grippe die Fähigkeit zum weitgehend unbehinderten Übertritt auf den Menschen verliehen haben sollen. Die Veränderung am Polymerase-Protein erlaubt es den Viren, längere Zeit als zuvor in der relativ kühlen Nase eines Menschen zu überdauern, während das veränderte Rezeptorprotein eine erleichterte Bindung an die Schleimhautzellen der Nase ermöglicht. Ob durch diese Kombination der Genveränderungen auch das Ausbreitungsverhalten der Viren verändert wird, ist derzeit ungeklärt.
Die Weltgesundheitsorganisation hat diese Befunde im Februar 2006 allerdings insoweit relativiert, als sie darauf hinwies, dass man derzeit nicht wisse, welche spezifischen Mutationen nötig seien, damit H5N1 leichter und nachhaltig von Mensch zu Mensch übergehen könne. Man wisse zum Beispiel auch nicht, ob es dem Fehlen eines spezifischen Rezeptors für dieses Virus im Menschen zu verdanken sei, dass es ihm derzeit nicht gelinge, sich effizient von Mensch zu Mensch zu verbreiten. Auch könne man künftige Veränderungen von Influenza-Viren nicht vorhersagen, so dass Aussagen über die Wahrscheinlichkeit oder den Zeitpunkt von Veränderungen, die zu einer Pandemie führen könnten, "schwierig wenn nicht unmöglich" seien. Aus diesen Gründen könne die Bedeutung von nachgewiesenen Mutationen nur im Zusammenhang mit beobachtbaren Krankheitsfällen, das heißt auf der Basis epidemiologischer Daten eingeschätzt werden. Die WHO empfahl daher, auch weiterhin jeden Erkrankungsfall beim Menschen sorgfältig zu untersuchen. [5]
Chinesischen Forschern ist es einer im Februar 2006 veröffentlichten Studie zufolge offenbar gelungen, den Entstehungsort der hochpathogenen H5N1-Variante einzugrenzen. Die Forscher hatten seit Anfang 2004 bis Mitte 2005 auf Märkten in sechs südostchinesischen Provinzen mehr als 51.000 Enten, Gänse und Hühner untersucht und dabei festgestellt, dass ungefähr 2 von 100 Enten und Gänsen das Virus unauffällig in sich trugen. Auch in einigen Hühnern (0,26 %) kam das Virus vor. Sie konnten ferner drei regionale Cluster (Unterschiede) in den Genen der Viren nachweisen, und zwar mit Schwerpunkt in den südchinesischen Provinzen Guangdong, Hunan und Yunnan. Diese Unterschiede deuten den Forschern zufolge darauf hin, dass die Viren schon geraume Zeit zur Verfügung hatten, um sich zu verändern. Die chinesischen Forscher vermuten, dass H5N1 bereits seit mehr als 10 Jahren in Südchina zirkuliert, obwohl es erst 1997 den ersten großen Ausbruch in der Geflügelhaltung gegeben hat. Im Gegensatz zu den offiziellen politischen Institutionen Chinas gehen die Forscher auch davon aus, dass sich die Viren in Südchina in die heute bestehende hoch pathogene Variante entwickelt haben und von dort in die Nachbarstaaten gelangt sind; Virusproben aus Thailand ähneln nämlich sehr stark den Proben aus Guangdong. [6]
Der beachtliche Durchseuchungsgrad der chinesischen Geflügelbestände mit A/H5N1 wird von Forschern auf die dort übliche Impfung vieler Tiere gegen Geflügelpest-Viren zurückgeführt, aufgrund derer viele Virusträger vor auffälligen Krankheitssymptomen geschützt sind.
Der Virologe Albert Osterhaus von der Erasmus Universität in Rotterdam, Niederlande, stellt zusammenfassend fest, dass sich die H5N1-Stämme von Anfang 2006 bereits deutlich von denen aus dem Jahr 1997 unterscheiden.
Ein Forscherteam um James Steavens vom Scripps Research Institute in La Jolla, Kalifornien, ist der Ansicht, dass die Influenza A/H5N1-Viren inzwischen den Erregern der humanen Influenza stärker ähneln, als bislang vermutet. Die Oberflächeneiweiße von H5N1 würden mittlerweile mit denen der Erreger der Spanischen Grippe auffallende Ähnlichkeiten aufweisen. Bei dem im Jahre 1997 bei Enten isolierten H5N1-Stamm konnten sie weniger Gemeinsamkeiten feststellen. Sie befürchten daher, dass nur noch wenige weitere Veränderungen auf der Oberflache der A/H5N1-Viren ausreichen könnten, um sie hoch gefährlich für den Menschen zu machen.
Impfstoffentwicklung
Aktive Immunisierung

Sowohl ein Forscherteam um Andrea Gambotto der University of Pittsburgh wie auch eine Gruppe um Suryaprakash Sambhara vom National Center of Disease Control and Prevention (CDC) in Atlanta, beide USA, haben Anfang Februar 2006 neuartige Prototypen eines bislang bei Mäusen und Hühnern zuverlässig wirksamen Vogelgrippe-Impfstoffs gegen A/H5N1 vorgestellt.
Die Mitarbeiter von Andrea Gambotto nahmen harmlose Erkältungsviren (Adenoviren) und bauten diesen ein spezielles Gen des A/H5N1-Virus ein, das auf der Virusoberfläche Teile oder die Vollversion eines bestimmten Proteins des Vogelgrippevirus herstellt (exprimiert). Dabei handelt es sich um das so genannte Hämagglutinin (HA), welches sich auf der Oberfläche aller Grippeviren findet und ihnen dabei hilft, an die Wirtszellen anzudocken, damit sie anschließend in sie eindringen können.

Bei Mäusen, die mit derart gentechnisch erzeugtem Impfstoff behandelt wurden, waren sechs Tage nach der anschließenden Infektion mit der Virusvariante A/Vietnam/H5N1/1203/2004 keine Erreger mehr nachweisbar, und nach 70 Tagen war auch eine Immunität gegenüber A/H5N1 zu beobachten. Hühner waren sogar schon nach 21 Tagen vor einer Vogelgrippe geschützt, wenn ihnen dieser Impfstoff unter die Haut (subkutan) gespritzt wurde. Nach Aussagen der Wissenschaftler basiert der Wirkstoff auf gentechnisch veränderten Komponenten des lebenden Virus und aktiviere daher das Immunsystem effektiver als herkömmliche Grippeimpfungen.
Da die für den neuen Impfstoff verwendeten veränderten Viren nicht wie die herkömmlichen Grippe-Impfstoffe in befruchteten Hühnereiern, sondern in Zellkulturen gezüchtet werden, könne man sie nunmehr sehr schnell und in großen Mengen produzieren und auch ebenso schnell auf erfolgte Virusveränderungen zuschneiden. Damit sei eine vereinfachte und beschleunigte Impfstoffherstellung möglich geworden. Nach eigenen Angaben benötigten die Wissenschaftler in Pittsburgh nur 36 Tage bis zur Produktion ihrer Seren.
Die Forscher um Suryaprakash Sambhara in Atlanta benutzten ebenfalls Erkältungsviren als "Transporter" für ein Gen des Virus. Bei ihnen überlebten alle mit diesem Impfstoff behandelten Mäuse eine anschließende Infektion mit A/H5N1, wobei sämtliche Viren innerhalb von vier Tagen in den Lungen der Tiere nicht mehr nachweisbar waren. Nach Angaben der Wissenschaftler sei ihr Impfstoff für verschiedene Untervarianten des Vogelgrippe-Virus einsetzbar und von den Mitarbeitern innerhalb von fünf bis sieben Wochen herzustellen.
Experten sind allerdings der Ansicht, dass noch viele zeitaufwändige Tests notwendig sind, bis eine wirksame Impfung von Menschen möglich wird. So könnten bis zur Marktreife der Impfstoffe drei bis vier Jahre vergehen.
Ein Forscherteam um John Treanor von der University of Rochester, US-Bundesstaat New York, hat Anfang 2006 einen auf herkömmliche Weise in Hühnereiern hergestellten Impfstoff gegen H5N1 auf seine Wirksamkeit beim Menschen getestet. Im Gegensatz zu der bei Impfstoffen gegen die humane Influenza verwendeten Dosis von 15 Mikrogramm erhielten die Probanden von diesen Wissenschaftlern nunmehr zwei Impfungen mit entweder 7,5 oder aber 90 Mikrogramm im Abstand von vier Wochen. In der Hochdosisgruppe erreichten 54 Prozent der Probanden nach der zweiten Impfung einen mittels Blutproben festgestellten Antikörperspiegel, der nach Expertenvermutung vermutlich vor einer Erkrankung schützt. Allerdings bewertet der Forscher Gregory Poland von der Mayo Klink in Rochester die von seinen Kollegen erzielte Schutzwirkung beim Menschen als schwach oder höchstens mittelmäßig. Außerdem weist er darauf hin, dass man für die mittlerweile kursierenden unterschiedlichen Varianten von H5N1 auch mit Sicherheit mehrere unterschiedliche Vakzine benötigt. Deshalb hält Poland viel eher die Förderung von moderneren Impfstoffproduktionsverfahren mittels Zellkulturen für erforderlich.
Ein Team um Thomas Mettenleiter vom Friedrich-Löffler Institut auf der Insel Riem hat unlängst den Prototypen für einen Impfstoff gegen Vogelgrippe entwickelt, der Hühner vor dieser Viruserkrankung schützt und im Gegensatz zu herkömmlichen Impfstoffen eine eindeutige Unterscheidung von geimpften und infizierten Tieren erlaubt [7].
Für ihre Experimente wandelten die Forscher ein vorhandenes Vakzin aus abgetöteten Nwecastle Disease Viren (NDV) gegen die Newcastle-Krankheit geringfügig ab, in dem sie in das Erbgut dieser Viren ein Gen des Vogelgrippevirus einbauten. Versuche bei Hühnern deuteten darauf hin, dass der neue Impfstoff sowohl vor der Newcastle-Krankheit wie auch der Vogelgrippe schützt, da diese so behandelten Tiere anschließend die Infektion hoher Mengen von Vogelgrippe- und ND-Viren überstanden und Antikörper gegen beide Erregerarten bildeten. Allerdings entstanden hierbei andere Antikörper als nach einer herkömmlichen Vogelgrippe-Impfung oder Direktinfektion, weshalb nunmehr eine klare Unterscheidung zwischen geimpften und infizierten Tieren möglich wird. Der neue Impfstoff soll in weiteren Tests überprüft werden und kann jedoch Günstigenfalls frühestens in etwa fünf Jahren zugelassen werden
Passive Immunisierung
Anfang 2006 hat ein Forschungsteam um Jaihai Lu von der Sun Yat-sen Universität in Guanzhou, Volksrepublik China, eine passive Impfung gegen H5N1 für Mäuse entwickelt. Die Forscher infizierten Pferde mit abgeschwächten H5N1-Viren und extrahierten anschließend die gegen diese Erreger gebildeten Antikörper aus ihrem Blut. Danach schnitten sie mit einem Enzym ein bestimmtes Fragment aus diesen Antikörpern, welches von dem Immunsystem der Mäuse nicht abgestoßen wird. Dieses Antikörperfragment wurde nun Mäusen injiziert, die 25 Stunden zuvor mit einer für sie normalerweise tödlichen H5N1-Virusdosis infiziert worden waren. Nach Angaben der chinesischen Forscher schützten 100 Mikrogramm der Antikörperfragmente alle Mäuse vor dem sonst sicheren Tod, denn sämtliche nur mit einem Placebo behandelten Tiere der Kontrollgruppe verstarben in der Regel nach etwa neun Stunden. Experten äußern jedoch hinsichtlich einer möglichen Anwendung dieses Verfahrens beim Menschen erhebliche Bedenken, da ein solcher passiver Impfstoff sich zwar schneller herstellen ließe als ein aktiver, er aber andererseits eine schlechtere Verträglichkeit besitzen und nur einen geringeren Immunschutz bewirken würde.
Quellen und Anmerkungen
- ↑ siehe Vogelgrippe#Ausbreitung bis Ende 2005 und Influenza A/H5N1: Ausbreitung 1997-2005
- ↑ Nature Bd 440, S. 435
- ↑ [1], [2]
- ↑ Nature Bd 439 vom 19. Januar 2006, S. 248 f.
- ↑ http://www.who.int/csr/2006_02_20/en/index.html
- ↑ Science Bd. 311 vom 3.3.06, S. 1225
- ↑ http://www.pnas.org/cgi/content/abstract/103/21/8197
Literatur
- Xiyan Xu u.a.: Genetitic characterization of the pathogenic Influenza A/Goose/Guangdong/1/96 (H5N1) Virus: Similarity of its hemagglutinin gene to those of H5N1 viruses from the 1997 outbreak in Hong Kong. In: Virology 261, 15-19 (1999)
Weblinks
- Robert-Koch-Institut: Vorgehen bei Verdacht auf Erkrankung eines Menschen (pdf)
- Friedrich-Loeffler-Institut: Antworten auf Fragen zur hoch pathogenen Aviären Influenza (HPAI, Geflügelpest, „Vogelgrippe“) (pdf)
- www.oie.int Aktuelle Daten zur weltweiten Situation bezüglich der aviären Influenza (englisch)
- H5N1 bei NCBI




