Colistin
| Strukturformel | |||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
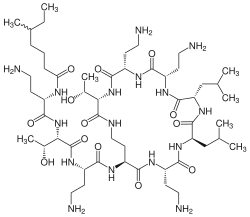
| |||||||||||||
| Allgemeines | |||||||||||||
| Freiname | Colistin | ||||||||||||
| Andere Namen |
Polymyxin E | ||||||||||||
| Summenformel | C52H98N16O13 | ||||||||||||
| Externe Identifikatoren/Datenbanken | |||||||||||||
| |||||||||||||
| Arzneistoffangaben | |||||||||||||
| ATC-Code | |||||||||||||
| Wirkstoffklasse | |||||||||||||
| Wirkmechanismus |
Störung der Permeabilität der Zellmembran | ||||||||||||
| Eigenschaften | |||||||||||||
| Molare Masse | 1155,43 g·mol−1 | ||||||||||||
| Sicherheitshinweise | |||||||||||||
| |||||||||||||
| Toxikologische Daten | |||||||||||||
| Soweit möglich und gebräuchlich, werden SI-Einheiten verwendet. Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen (0 °C, 1000 hPa). | |||||||||||||
Colistin (auch Polymyxin E) ist ein Antibiotikum aus der Gruppe der Polymyxine. Das 1950 erstmals von S. Kayama aus Bacillus colistinus[3] gewonnene Polymyxin steht seit 1959 zur Therapie zur Verfügung.[4]
Anwendung
Colistin wurde wegen seiner Toxizität bei systemischer Anwendung lange hauptsächlich lokal als Salbenzusatz, oral zur Darmbehandlung oder als Aerosol zur Inhalationstherapie eingesetzt, insbesondere bei Mukoviszidose mit chronischer Pseudomonas-Besiedelung.[5]
Für die parenterale systemische Therapie beim Menschen gibt es seit dem Jahr 2012 in Deutschland wieder zugelassene Fertigarzneimittel.[6] Hintergrund für die Renaissance des als vor allem nephrotoxisch geltenden Antibiotikums[7] ist das gehäufte Auftreten Carbapenem-resistenter Enterobakterien (sogenannte „CRE“; derzeit vor allem in den USA, Israel, Griechenland, Türkei und nordafrikanischen Ländern). Die Therapieoptionen für CRE sind meist beschränkt auf Colistin, Fosfomycin und Tigecyclin.[8]
Auch in der Tiermedizin wird der Wirkstoff bei Schweinen und Rindern mit schweren Septikämien parenteral angewendet.[9] Im mikrobiologischen Labor wird die Substanz in Nährböden zur Selektion grampositiver Bakterien eingesetzt (häufig in Kombination mit Nalidixinsäure), da Colistin das Wachstum vieler gramnegativer Bakterien hemmt, nicht jedoch das grampositiver Bakterien.
Analytik
Da Colistin als Reserveantibiotikum gilt, ist der sichere qualitative und quantitative Nachweis der Substanz von besonderer Bedeutung. Für den zuverlässigen Nachweis in Plasma und Urin stehen heute die Kopplungen der HPLC mit der Massenspektrometrie nach hinreichender Probenvorbereitung zur Verfügung.[10][11] Für sehr komplexe Untersuchungsmaterialien, wie z. B. Schweineexkremente sind besonders aufwändige Vorbereitungen erforderlich.[12] Auch für die Untersuchung von Muskelgewebe stehen hochspezifische Nachweise mit angemessener Probenvorbereitung zur Verfügung.[13]
Wirkungsmechanismus
Colistimethat-Natrium (CMS) ist ein so genanntes Prodrug, welches nach parenteraler Applikation zunächst durch Hydrolyse in die pharmakologisch aktive Colistin-Base umgewandelt wird. Aus 80 mg CMS (= 1 Mio. I.E.). werden ca. 33 mg Colistin-Base freigesetzt.[14] Colistin wirkt über eine Schädigung der äußeren Membran auf gramnegative Bakterien.[15]
- empfindlich: Salmonellen, Shigellen, Haemophilus influenzae, Pasteurellen, Acinetobacter
- meist empfindlich: Pseudomonas aeruginosa, Escherichia coli, Enterobacter, Klebsiellen
- resistent: Proteus, Gonokokken, Meningokokken und grampositive Bakterien
Mit Polymyxin B besteht eine Kreuzresistenz.
Resistenz
Colistin gilt als Reserveantibiotikum für die Behandlung von multiresistenten Acinetobacter baumannii. Auf Intensivstationen werden immer häufiger Resistenzen beschrieben, wobei es weltweit keinen einheitlichen Grenzwert (MHK) für die Resistenzbeschreibung gibt.[16][17][18] Eine Form der Resistenz wurde zunächst in Nutztieren,[19][20] inzwischen aber auch in menschlichen E. coli-Bakterien gefunden.[21] Ausgelöst wird die Resistenz durch das Gen MCR-1.
Nebenwirkungen
- Neuro- und Nephrotoxizität insbesondere bei systemischer Anwendung. Die Nephrotoxizität ist besonders ausgeprägt bei Personen mit niedrigen Werten von Serumalbumin.[22]
- Kontaktdermatitis bei Anwendung als Salbe
- Asthmaanfälle bei Inhalation
Wechselwirkungen
Verstärkung der Nebenwirkungen mit nephrotoxischen Wirkstoffen (etwa Aminoglykosiden, Vancomycin und Schleifendiuretika) und Wirkstoffen mit neuromuskulärer Blockade (wie Muskelrelaxantien)
Gegenanzeigen
Überempfindlichkeit gegen Colistin oder Polymyxin B.
Bei Nierenschäden ist eine Dosisanpassung (anhand der gemessenen Kreatinin-Clearance) notwendig.
Rechtliches
Colistin ist verschreibungspflichtig und damit auch apothekenpflichtig.
Handelsnamen
Humanmedizin:
- Zur oralen Gabe: Diarönt mono (D), als Generikum (D, CH)[23][24]
- Zur Inhalation: Colistin CF (D), Promixin (D), ColiFin (D), Colistineb (D)[23]
- Zur i.v.-Gabe: Promixin (D), Colistimethat-Natrium INFECTOPHARM 1 Mio. I.E. (D)[23]
- Zur Inhalation und i.v.-Gabe: ColistiFlex (D)[23]
Tiermedizin: Animedistin, Belacol, Carbophen, Coliplus, Colipur, Colivet, Enteroxid, Klato Col, Colistinsulfat 100%
Literatur
- M. E. Falagas, S. K. Kasiakou, S. Tsiodras, A. Michalopoulos: The use of intravenous and aerosolized polymyxins for the treatment of infections in critically ill patients: a review of the recent literature. In: Clin Med Res. Band 4, Nr. 2, Juni 2006, S. 138–146, PMID 16809407, PMC 1483888 (freier Volltext).
- M. E. Falagas, S. K. Kasiakou: Toxicity of polymyxins: a systematic review of the evidence from old and recent studies. In: Crit Care. Band 10, Nr. 1, Februar 2006, S. R27, doi:10.1186/cc3995, PMID 16507149, PMC 1550802 (freier Volltext).
Einzelnachweise
- ↑ a b Datenblatt Colistin sulfate salt bei Sigma-Aldrich, abgerufen am 23. März 2011 (PDF).
- ↑ Antibiotiki., 5(4)(10), 1960.
- ↑ Karl Wurm, A. M. Walter: Infektionskrankheiten. In: Ludwig Heilmeyer (Hrsg.): Lehrbuch der Inneren Medizin. Springer-Verlag, Berlin/Göttingen/Heidelberg 1955; 2. Auflage ebenda 1961, S. 9–223, hier: S. 55.
- ↑ Kurzbeschreibung Colistin In: Zeitschrift für Chemotherapie. Mai 2005.
- ↑ H. Heijerman, E. Westerman, S. Conway, D. Touw, G. Döring: Inhaled medication and inhalation devices for lung disease in patients with cystic fibrosis: A European consensus. In: J. Cyst. Fibros. Band 8, Nr. 5, September 2009, S. 295–315, doi:10.1016/j.jcf.2009.04.005, PMID 19559658.
- ↑ Fachinformation Promixin; Fachinformation Colistimethat-Natrium INFECTOPHARM 1 Mio. I.E.
- ↑ J. Li: Colistin-Induced Apoptosis in Rat Renal Proximal Tubular Cells: Concentration- and Time-dependence and Protection by Melatonin. Poster A2-1183, ICAAC 2011.
- ↑ A. Lerner: Environmental Spread of Carbapenem-Resistant Enterobacteriaceae (CRE) by Patients Known to be Colonized with CRE. Vortrag, ICAAC 2011
- ↑ W. Löscher u. a. (Hrsg.): Pharmakotherapie bei Haus- und Nutztieren. 7. Auflage. Paul Parey Verlag, 2006, ISBN 3-8304-4160-6, S. 266.
- ↑ K. Bihan, Q. Lu, M. Enjalbert, M. Apparuit, O. Langeron, J. J. Rouby, C. Funck-Brentano, N. Zahr: Determination of colistin and colistimethate levels in human plasma and urine by high-performance liquid chromatography-tandem mass spectrometry. In: Ther Drug Monit. 38(6), 27. Sep 2016, S. 796–803. PMID 27684296
- ↑ M. Zhao, X. J. Wu, Y. X. Fan, B. N. Guo, J. Zhang: Development and validation of a UHPLC-MS/MS assay for colistin methanesulphonate (CMS) and colistin in human plasma and urine using weak-cation exchange solid-phase extraction. In: J Pharm Biomed Anal. 124, 30. Mai 2016, S. 303–308. PMID 26970986
- ↑ T. Van den Meersche, E. Van Pamel, C. Van Poucke, L. Herman, M. Heyndrickx, G. Rasschaert, E. Daeseleire: Development, validation and application of an ultra high performance liquid chromatographic-tandem mass spectrometric method for the simultaneous detection and quantification of five different classes of veterinary antibiotics in swine manure. In: J Chromatogr A., 1429, 15. Januar 2016, S. 248–257. PMID 26739912
- ↑ J. O. Boison, S. Lee, J. Matus: A multi-residue method for the determination of seven polypeptide drug residues in chicken muscle tissues by LC-MS/MS. In: Anal Bioanal Chem. 407(14), Mai 2015, S. 4065–4078. PMID 25832483
- ↑ K. de With, H. Stocker, J. Borde, W. V. Kern: Antibiotika – neue und alte Substanzen, rationale Verordnung. In: Dtsch med Wochenschr. 137, 2012, S. 186–189.
- ↑ N. P. Mortensen, J. D. Fowlkes, C. J. Sullivan u. a.: Effects of colistin on surface ultrastructure and nanomechanics of Pseudomonas aeruginosa cells. In: Langmuir. Band 25, Nr. 6, April 2009, S. 3728–3733, doi:10.1021/la803898g, PMID 19227989.
- ↑ Anastasia Antoniadou, Flora Kontopidou, Garifalia Poulakou, Evangelos Koratzanis, Irene Galani, Evangelos Papadomichelakis, Petros Kopterides, Maria Souli, Apostolos Armaganidis, Helen Giamarellou: Colistin-resistant isolates of Klebsiella pneumoniae emerging in intensive care unit patients: first report of a multiclonal cluster. In: J. Antimicrob. Chemother. 59 (4), 2007, S. 786–790. doi:10.1093/jac/dkl562
- ↑ Yun Cai, Dong Chai, Rui Wang, Beibei Liang, Nan Bai: Colistin resistance of Acinetobacter baumannii: clinical reports, mechanisms and antimicrobial strategies. In: J. Antimicrob. Chemother., 2012. doi:10.1093/jac/dks084
- ↑ Acinetobacter baumannii – Studie. Robert Koch-Institut.
- ↑ Fragen und Antworten zum Antibiotikum Colistin und zur übertragbaren Colistin-Resistenz von Bakterien - BfR. Abgerufen am 26. Februar 2024.
- ↑ Übertragbare Colistin-Resistenz in Keimen von Nutztieren in Deutschland. BfR, 7. Januar 2016.
- ↑ Das bedeutet der „Super-Erreger“-Fund. MCR-1 schaltet antibiotika aus. In: Spiegel Online. 27. Mai 2015, abgerufen am 16. August 2017.
- ↑ Daniele Roberto Giacobbe, Alessandra di Masi, Loris Leboffe, Valerio Del Bono, Marianna Rossi, Dario Cappiello, Erika Coppo, Anna Marchese, Annarita Casulli, Alessio Signori, Andrea Novelli, Katja Perrone, Luigi Principe, Alessandra Bandera, Luca Enrico Vender, Andrea Misin, Pierpaolo Occhilupo, Marcello Melone, Paolo Ascenzi, Andrea Gori, Roberto Luzzati, Claudio Viscoli, Stefano Di Bella: Hypoalbuminemia as a predictor of acute kidney injury during colistin treatment. In: Scientific Reports. Band 8, Nr. 1, 10. August 2018, doi:10.1038/s41598-018-30361-5, PMID 30097635, PMC 6086859 (freier Volltext).
- ↑ a b c d Rote Liste online, Stand: Februar 2016.
- ↑ AM-Komp. d. Schweiz, Stand: Oktober 2009.




