„Doxorubicin“ – Versionsunterschied
| [gesichtete Version] | [gesichtete Version] |
Leerzeichen vor/nach Schrägstrich korrigiert |
|||
| (13 dazwischenliegende Versionen von 7 Benutzern werden nicht angezeigt) | |||
| Zeile 5: | Zeile 5: | ||
| Andere Namen = * Hydroxyldaunorubicin |
| Andere Namen = * Hydroxyldaunorubicin |
||
* Adriamycin |
* Adriamycin |
||
* (7''S'',9''S'')-7-[(2''R'',4''S'',5''S'',6''S'')-4-Amino-5-hydroxy-6-methyloxan-2-yl]oxy-6,9,11-trihydroxy-9-(2-hydroxyacetyl)-4-methoxy-8,10-dihydro-7''H''-tetracen-5,12-dion <small>([[IUPAC]])</small> |
* (7''S'',9''S'')-7-[(2''R'',4''S'',5''S'',6''S'')-4-Amino-5-hydroxy-6-methyloxan-2-yl]oxy-6,9,11-trihydroxy-9-(2-hydroxyacetyl)-4-methoxy-8,10-dihydro-7''H''-tetracen-5,12-dion <small>([[IUPAC-Nomenklatur|IUPAC]])</small> |
||
| Summenformel = * C<sub>27</sub>H<sub>29</sub>NO<sub>11</sub> <small>(Doxorubicin)</small> |
| Summenformel = * C<sub>27</sub>H<sub>29</sub>NO<sub>11</sub> <small>(Doxorubicin)</small> |
||
* C<sub>27</sub>H<sub>29</sub>NO<sub>11</sub>·HCl <small>(Doxorubicin·Hydrochlorid)</small> |
* C<sub>27</sub>H<sub>29</sub>NO<sub>11</sub>·HCl <small>(Doxorubicin·Hydrochlorid)</small> |
||
| CAS = * 23214-92-8 |
| CAS = * {{CASRN|23214-92-8}} |
||
* 25316-40-9 ([[Hydrochlorid]]) |
* {{CASRN|25316-40-9|Q27032359}} ([[Hydrochlorid]]) |
||
| EG-Nummer = |
| EG-Nummer = 245-495-6 |
||
| ECHA-ID = |
| ECHA-ID = 100.041.344 |
||
| PubChem = 31703 |
| PubChem = 31703 |
||
| ChemSpider = |
| ChemSpider = 29400 |
||
| ATC-Code = {{ATC|L01|DB01}} |
| ATC-Code = {{ATC|L01|DB01}} |
||
| DrugBank = DB00997 |
| DrugBank = DB00997 |
||
| Zeile 25: | Zeile 25: | ||
| Siedepunkt = |
| Siedepunkt = |
||
| Dampfdruck = |
| Dampfdruck = |
||
| pKs = 8,2<ref>{{RömppOnline|Name=Doxorubicin |
| pKs = 8,2<ref>{{RömppOnline|ID=RD-04-02493|Name=Doxorubicin|Abruf=2019-06-25}}</ref> |
||
| Löslichkeit = leichtlöslich in Wasser, Methanol, Acetonitril und Tetrahydrofuran<small>(Doxorubicin·Hydrochlorid)</small><ref name="MERCK_Index" /> |
| Löslichkeit = leichtlöslich in Wasser, Methanol, Acetonitril und Tetrahydrofuran<small>(Doxorubicin·Hydrochlorid)</small><ref name="MERCK_Index" /> |
||
| Quelle GHS-Kz = <ref name="Sigma">{{Sigma-Aldrich|SIGMA|D1515 |
| Quelle GHS-Kz = <ref name="Sigma">{{Sigma-Aldrich|SIGMA|D1515|Name=Doxorubicin hydrochloride|Abruf=2022-05-29}}</ref> |
||
| GHS-Piktogramme = Hydrochlorid<br />{{GHS-Piktogramme-klein|07|08}} |
| GHS-Piktogramme = Hydrochlorid<br />{{GHS-Piktogramme-klein|07|08}} |
||
| GHS-Signalwort = Gefahr |
| GHS-Signalwort = Gefahr |
||
| H = {{H-Sätze|302|350}} |
| H = {{H-Sätze|302|340|350|360FD}} |
||
| EUH = {{EUH-Sätze|-}} |
| EUH = {{EUH-Sätze|-}} |
||
| P = {{P-Sätze|201|308+313}} |
| P = {{P-Sätze|201|202|264|270|301+312|308+313}} |
||
| Quelle P = <ref name="Sigma" /> |
| Quelle P = <ref name="Sigma" /> |
||
| ToxDaten = {{ToxDaten |Typ=LD50 |Organismus=Maus |Applikationsart=oral |Wert=570 mg·kg<sup>−1</sup> |Bezeichnung= |Quelle=<ref name="ChemIDplus">{{ChemID|23214-92-8}} |
| ToxDaten = {{ToxDaten |Typ=LD50 |Organismus=Maus |Applikationsart=oral |Wert=570 mg·kg<sup>−1</sup> |Bezeichnung= |Quelle=<ref name="ChemIDplus">{{ChemID|CAS=23214-92-8|Name=Doxorubicin|Abruf=}}</ref> }} |
||
}} |
}} |
||
'''Doxorubicin''' ist das [[Hydroxygruppe|Hydroxy]][[Derivat (Chemie)|derivat]] des [[Daunorubicin]] und gehört zur Stoffgruppe der [[Anthracycline]]. |
'''Doxorubicin''' ist das [[Hydroxygruppe|Hydroxy]][[Derivat (Chemie)|derivat]] des [[Daunorubicin]] und gehört zur Stoffgruppe der [[Anthracycline]]. Die Verbindung ist ein [[Stereoisomer]] von [[Epirubicin]] und wird als stereochemisch reiner [[Arzneistoff]] in der [[Chemotherapie]] ([[Zytostatikum]]) eingesetzt. Doxorubicin gehört zur Wirkstoffgruppe der [[Zytostatikum#Interkalantien|Interkalantien]]. Die Wirkung beruht auf der [[Interkalation (Chemie)|Interkalation]] in die [[Desoxyribonukleinsäure|DNA]]. |
||
== Eigenschaften == |
== Eigenschaften == |
||
| Zeile 53: | Zeile 53: | ||
== Handelsnamen == |
== Handelsnamen == |
||
| ⚫ | |||
[[Monopräparat]]e Doxorubicin: |
|||
* Liposomal verkapseltes Doxorubicin: ''Myocet'' (EU<ref name="emamyocet">[https://www.ema.europa.eu/en/medicines/human/EPAR/myocet-liposomal-previously-myocet Myocet liposomal (previously Myocet)], EMA, abgerufen am 1. April 2022.</ref>) |
|||
| ⚫ | |||
* Pegyliertes liposomal verkapseltes Doxorubicin: ''Caelyx'' (EU,<ref name="ema">[https://www.ema.europa.eu/en/medicines/human/EPAR/caelyx-pegylated-liposomal Caelyx pegylated liposomal], EMA, abgerufen am 1. April 2022.</ref> CH) |
|||
Monopräparat liposomal-verkapseltes Doxorubicin: Myocet<ref name="Rote Liste">Rote Liste Service GmbH (Hrsg.): ''Rote Liste 2017 – Arzneimittelverzeichnis für Deutschland (einschließlich EU-Zulassungen und bestimmter Medizinprodukte)'', Rote Liste Service GmbH, Frankfurt/Main, 2017, Aufl. 57, ISBN 978-3-946057-10-9, S. 1286.</ref> (D, A) |
|||
Monopräparat PEG-liposomal-verkapseltes Doxorubicin: Caelyx (D, A, CH) |
|||
== Literatur == |
== Literatur == |
||
* M. Ghione, J. Fetzer, H. Maier (Hrsg.): ''Ergebnisse der Adriamycin-Therapie''. Adriamycin-Symposium, Frankfurt am Main 1974. Springer, Berlin/ Heidelberg/ New York 1975. |
* M. Ghione, J. Fetzer, H. Maier (Hrsg.): ''Ergebnisse der Adriamycin-Therapie''. Adriamycin-Symposium, Frankfurt am Main 1974. Springer, Berlin / Heidelberg / New York 1975. |
||
* J. Fetzer, D. Füllenbach, H. Gabel (Hrsg.): ''Adriamycin. Solide Tumoren, Hämoblastosen; neue Möglichkeiten der Chemotherapie''. Band 1–3. Kehrer, Freiburg i. Br. 1977–1980. |
* J. Fetzer, D. Füllenbach, H. Gabel (Hrsg.): ''Adriamycin. Solide Tumoren, Hämoblastosen; neue Möglichkeiten der Chemotherapie''. Band 1–3. Kehrer, Freiburg i. Br. 1977–1980. |
||
== Weblinks == |
== Weblinks == |
||
* [ |
* [https://www.clinicaltrials.gov/ct2/results?term=Doxorubicin Einträge im NIH-Studienregister] |
||
== Einzelnachweise == |
== Einzelnachweise == |
||
| Zeile 74: | Zeile 71: | ||
{{Normdaten|TYP=s|GND=4150505-0}} |
{{Normdaten|TYP=s|GND=4150505-0}} |
||
[[Kategorie: |
[[Kategorie:Tetrahydronaphthalin]] |
||
[[Kategorie:Dihydroxyanthrachinon]] |
[[Kategorie:Dihydroxyanthrachinon]] |
||
[[Kategorie: |
[[Kategorie:Hydrochinon]] |
||
[[Kategorie:Methoxybenzol]] |
|||
[[Kategorie:Hydroxyoxan]] |
|||
[[Kategorie:Beta-Aminoalkohol]] |
[[Kategorie:Beta-Aminoalkohol]] |
||
[[Kategorie:Hydroxyketon]] |
[[Kategorie:Hydroxyketon]] |
||
[[Kategorie: |
[[Kategorie:Acetal]] |
||
[[Kategorie:Zytostatikum]] |
[[Kategorie:Zytostatikum]] |
||
[[Kategorie:Arzneistoff]] |
[[Kategorie:Arzneistoff]] |
||
Aktuelle Version vom 14. Juni 2024, 23:05 Uhr
| Strukturformel | ||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
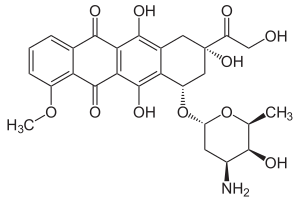
| ||||||||||||||||||||||
| Allgemeines | ||||||||||||||||||||||
| Freiname | Doxorubicin | |||||||||||||||||||||
| Andere Namen |
| |||||||||||||||||||||
| Summenformel |
| |||||||||||||||||||||
| Externe Identifikatoren/Datenbanken | ||||||||||||||||||||||
| ||||||||||||||||||||||
| Arzneistoffangaben | ||||||||||||||||||||||
| ATC-Code | ||||||||||||||||||||||
| Wirkstoffklasse | ||||||||||||||||||||||
| Wirkmechanismus | ||||||||||||||||||||||
| Eigenschaften | ||||||||||||||||||||||
| Molare Masse | ||||||||||||||||||||||
| Aggregatzustand |
fest | |||||||||||||||||||||
| Schmelzpunkt | ||||||||||||||||||||||
| pKS-Wert |
8,2[2] | |||||||||||||||||||||
| Löslichkeit |
leichtlöslich in Wasser, Methanol, Acetonitril und Tetrahydrofuran(Doxorubicin·Hydrochlorid)[1] | |||||||||||||||||||||
| Sicherheitshinweise | ||||||||||||||||||||||
| ||||||||||||||||||||||
| Toxikologische Daten | ||||||||||||||||||||||
| Soweit möglich und gebräuchlich, werden SI-Einheiten verwendet. Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen (0 °C, 1000 hPa). | ||||||||||||||||||||||
Doxorubicin ist das Hydroxyderivat des Daunorubicin und gehört zur Stoffgruppe der Anthracycline. Die Verbindung ist ein Stereoisomer von Epirubicin und wird als stereochemisch reiner Arzneistoff in der Chemotherapie (Zytostatikum) eingesetzt. Doxorubicin gehört zur Wirkstoffgruppe der Interkalantien. Die Wirkung beruht auf der Interkalation in die DNA.
Eigenschaften
Doxorubicin wirkt als Interkalans auf planare Verbindungen in DNA und RNA. Die DNA-Synthese wird gestört, Topoisomerase II gehemmt und es erfolgt eine Radikalbildung.
Doxorubicin besitzt Fluoreszenzeigenschaften, die dazu genutzt werden können, das Ausschleusen von Doxorubicin aus der Zelle zu untersuchen. Ein in solche Prozesse involviertes Protein ist das erstmals aus einer Doxorubicin-resistenten Lungenkrebs-Zelllinie klonierte MRP1 aus der Familie der ABC-Transporter. Ferner kann Doxorubicin auch eingesetzt werden, um die Lokalisation der an der Multiple Drug Resistance beteiligten Proteine und die Rolle der Organellen wie des Golgi-Apparats und der Lysosome zu klären.[3]
Anwendungen
Doxorubicin findet als Zytostatikum Anwendung bei der Behandlung von Tumoren wie z. B. Mammakarzinomen, Bronchialkarzinomen und Lymphomen. Das Medikament wird in diesen Indikationen intravenös verabreicht. Zur Behandlung insbesondere des hepatozellulären Karzinoms (HCC) wird es im Rahmen der transarteriellen Chemoembolisation (TACE) intraarteriell angewendet. Dazu wird es entweder in einer Emulsion mit einem öligen Kontrastmittel (Lipiodol) oder gebunden an medikamentenfreisetzende Partikel appliziert.
Nebenwirkungen
Die bedeutendsten Nebenwirkungen umfassen Knochenmarksdepression, Nephrotoxizität,[5] Kardiotoxizität (kumulativ dosisabhängige dilatative Kardiomyopathie), Ulcerationen und dermatotoxische Effekte. Es kann eine Anreicherung in tumorunabhängigem Gewebe wie etwa dem Herzen stattfinden, dem wird mittels einer PEGylierung entgegengewirkt, um die Spiegel im Plasma und Tumorgewebe zu konzentrieren.
Die effektivste Methode zur Verhinderung einer Doxorubicin-induzierten dilatativen Kardiomyopathie („Adriamycin-Kardiopathie“[6]), die auch noch Monate nach Verabreichung auftreten kann, ist die Gabe von Dexrazoxan.
Handelsnamen
- Adriblastin (D, A, CH), Adrimedac (D), Ribodoxo (D), diverse Generika (D, A, CH)
- Liposomal verkapseltes Doxorubicin: Myocet (EU[7])
- Pegyliertes liposomal verkapseltes Doxorubicin: Caelyx (EU,[8] CH)
Literatur
- M. Ghione, J. Fetzer, H. Maier (Hrsg.): Ergebnisse der Adriamycin-Therapie. Adriamycin-Symposium, Frankfurt am Main 1974. Springer, Berlin / Heidelberg / New York 1975.
- J. Fetzer, D. Füllenbach, H. Gabel (Hrsg.): Adriamycin. Solide Tumoren, Hämoblastosen; neue Möglichkeiten der Chemotherapie. Band 1–3. Kehrer, Freiburg i. Br. 1977–1980.
Weblinks
Einzelnachweise
- ↑ a b The Merck Index: An Encyclopedia of Chemicals, Drugs, and Biologicals. 14. Auflage. Merck & Co., Whitehouse Station, NJ, USA, 2006, ISBN 0-911910-00-X, S. 582.
- ↑ Eintrag zu Doxorubicin. In: Römpp Online. Georg Thieme Verlag, abgerufen am 25. Juni 2019.
- ↑ a b c Datenblatt Doxorubicin hydrochloride bei Sigma-Aldrich, abgerufen am 29. Mai 2022 (PDF).
- ↑ Eintrag zu Doxorubicin in der ChemIDplus-Datenbank der United States National Library of Medicine (NLM) (Seite nicht mehr abrufbar)
- ↑ S. Ayla, I. Seckin u. a.: Doxorubicin induced nephrotoxicity: protective effect of nicotinamide. In: International journal of cell biology. Band 2011, S. 390238. doi:10.1155/2011/390238. PMID 21789041. PMC 3140777 (freier Volltext).
- ↑ B. Kunkel, M. Kaltenbach, Paul Schölmerich: Erkrankungen des Endokards, Myokards und Perikards, Herztumoren und Herztraumen. In: Rudolf Gross, Paul Schölmerich, Wolfgang Gerok (Hrsg.): 1000 Merksätze Innere Medizin. Schattauer, Stuttgart/New York 1971; 4., völlig neu bearbeitete Auflage ebenda 1989 (= UTB für Wissenschaft / Uni-Taschenbücher. Band 522), ISBN 3-7945-1282-0, S. 90–96, hier: S. 93.
- ↑ Myocet liposomal (previously Myocet), EMA, abgerufen am 1. April 2022.
- ↑ Caelyx pegylated liposomal, EMA, abgerufen am 1. April 2022.




