„Fentanyl“ – Versionsunterschied
| [gesichtete Version] | [ungesichtete Version] |
Keine Bearbeitungszusammenfassung |
→Pharmakologie: Der zelluläre Wirkmechanismus gehört in den Artikel Opioid. Markierung: Zurückgesetzt |
||
| (Eine dazwischenliegende Version desselben Benutzers wird nicht angezeigt) | |||
| Zeile 102: | Zeile 102: | ||
== Pharmakologie == |
== Pharmakologie == |
||
{| class="wikitable" style="float: right; margin-left: 15px; text-align: center;" |
{| class="wikitable" style="float: right; margin-left: 15px; text-align: center;" |
||
|+ |
|+Affinität an drei Opioidrezeptortypen (Jahr 1994)<ref name="pmid8114680">{{cite journal | author = Raynor K, Kong H, Chen Y, Yasuda K, Yu L, Bell GI, Reisine T | title = Pharmacological characterization of the cloned kappa-, delta-, and mu-opioid receptors | journal = Molecular Pharmacology | volume = 45 | issue = 2 | pages = 330–334 | date = 1994-02 | pmid = 8114680 |language=en }}</ref> |
||
! colspan="3"|[[Bindungsaffinität|Affinitäten]], K<sub>i</sub> |
! colspan="3"|[[Bindungsaffinität|Affinitäten]], K<sub>i</sub> |
||
!Verhältnis |
!Verhältnis |
||
| Zeile 116: | Zeile 116: | ||
|1:>2564:654 |
|1:>2564:654 |
||
|} |
|} |
||
Fentanyl erzeugt seine analgetische Wirkung wie auch viele seiner Nebenwirkungen durch Aktivierung des μ-[[Opioidrezeptoren|Opioidrezeptors]] (MOR). Fentanyl ist etwa 50 bis 100 mal so [[Analgetische Potenz|potent]] wie [[Morphin]], was bedeutet, dass Fentanyl mit einem Hundertstel der Masse von Morphin die gleiche Intensität der Schmerzlinderung erreicht. Im Vergleich zu vielen anderen [[Opioide]]n hat Fentanyl einen schnellen [[Wirkungseintritt]]<ref name="Kelly">E. Kelly, K. Sutcliffe, D. Cavallo, N. Ramos-Gonzalez, N. Alhosan, G. Henderson: ''The anomalous pharmacology of fentanyl.'' In: ''British journal of pharmacology.'' Mai 2021, [[doi:10.1111/bph.15573]], PMID 34030211.</ref> und eine relativ kurze Wirkungsdauer.<ref name="Roewer">Norbert Roewer, Holger Thiel: ''Taschenatlas der Anästhesie''. ISBN 978-3-13-128784-7, 2010. S. 70ff.</ref> |
|||
Fentanyl bindet an den [[Opioidrezeptoren|Opioidrezeptor]] μ, der zu den [[G-Protein-gekoppelte Rezeptoren|G-Protein-gekoppelten Rezeptoren]] gehört.<ref name="Han 22" /><ref name="Vo">Quynh N. Vo, Paween Mahinthichaichan, Gregory F. Payne, Christopher R. Ellis: ''How μ-opioid receptor recognizes fentanyl.'' In: ''Nature Communications.'' 2021, Band 12, Nummer 1. [[doi:10.1038/s41467-021-21262-9]]. PMID 33579956, {{PMC|7881245}}.</ref> Die Struktur des Rezeptors mit gebundenem Fentanyl wurde [[elektronenmikroskop]]isch bestimmt ({{PDB2|8EF5}}).<ref>Y. Zhuang, Y. Wang, B. He, X. He, X. E. Zhou, S. Guo, Q. Rao, J. Yang, J. Liu, Q. Zhou, X. Wang, M. Liu, W. Liu, X. Jiang, D. Yang, H. Jiang, J. Shen, K. Melcher, H. Chen, Y. Jiang, X. Cheng, M. W. Wang, X. Xie, H. E. Xu: ''Molecular recognition of morphine and fentanyl by the human μ-opioid receptor.'' In: ''[[Cell (Zeitschrift)|Cell]].'' Band 185, Nummer 23, November 2022, S. 4361–4375.e19, [[doi:10.1016/j.cell.2022.09.041]], PMID 36368306.</ref> Fentanyl ist etwa 70 bis 100<ref name="Palliativmedizin. 2009">[[Eberhard Klaschik]]: ''Schmerztherapie und Symptomkontrolle in der Palliativmedizin.'' 2009, S. 233 f.</ref> mal so [[Analgetische Potenz|potent]] wie [[Morphin]] (gemessen an der Masse ist nur ein Hundertstel der Menge an Fentanyl nötig, um die gleiche Wirkung zu erzielen) und besitzt eine höhere Wirksamkeit (das Wirkungsmaximum ist höher), während seine Wirkdauer in der Regel deutlich kürzer ist. Fentanyl wirkt bei einer [[intravenös]]en Gabe nach fünf bis 120<ref>D. Häske und andere: ''Analgesie bei Traumapatienten in der Notfallmedizin.'' In: ''Der Anaesthesist'', Band 69, Nr. 2, Februar 2020, S. 137–148, hier: S. 141 (Wirkbeginn bei 0,6–2,5 µg/kgKG und intravenöser Gabe: 1–2 Minuten).</ref> Sekunden analgetisch. Die maximale Wirkung tritt nach vier bis fünf Minuten ein. Die [[biologische Halbwertszeit]] liegt bei ein bis zwei Stunden.<ref>James M. Ritter, Rod Flower, Graeme Henderson, Yoon Kong Loke, David MacEwan, and Humphrey P. Rang: ''Rang & Dale's Pharmacology''. 9. Auflage 2020. Elsevier. ISBN 978-0-7020-7448-6. S. 556.</ref> Die Berechnung von Dosierungsschemata für in der Anästhesie intravenös verabreichte Opioide erfordert jedoch eine komplexere Berücksichtigung ihres pharmakokinetischen Verhaltens, welches in der Literatur mit Multikompartimentmodellen beschrieben wird.<ref name="gupta2011">D.K. Gupta, T.C. Krejcie, M.J. Avram: ''Pharmacokinetics of opioids''. In: ''Anesthetic Pharmacology'' (Hrsg.: A.S. Evers, M. Maze, E.D. Kharasch) Cambridge University Press, 2011. S. 509–530. [[doi:10.1017/cbo9780511781933.033]]</ref> Demnach fällt nach intravenöser Injektion die Fentanyl-Plasmakonzentration in drei Phasen unterschiedlich rasch ab, deren Halbwertszeiten rund 1 Minute, 19 Minuten und 7,9 Stunden betragen.<ref name="gupta2011" /> Die zur Behandlung effektive Dosis ([[Effektivdosis|ED<sub>50</sub>]]) liegt bei 2 bis 20 µg/kg Körpergewicht bei laufender Überwachung der Atmung. Nach Bindung von Fentanyl an den Opioidrezeptor μ werden nicht nur [[G-Protein]]e vom Typ G<sub>I/0</sub> aktiviert, sondern auch [[β-Arrestin]].<ref name="Comer" /> Die Aktivierung der G<sub>I/0</sub> führt zur Hemmung der [[Adenylylcyclase]].<ref name="Udayakumar">P. Udayakumar, S. Udayakumar: ''Fentanyl-Induced Respiratory Depression: A Narrative Review on the Possible Single-Nucleotide Polymorphism.'' In: ''Anesthesia, essays and researches.'' Band 15, Nummer 1, 2021, S. 4–7, {{DOI|10.4103/aer.aer_94_21}}, PMID 34667340, {{PMC|8462425}}.</ref> Dadurch wird weniger [[Cyclisches Adenosinmonophosphat|cAMP]] gebildet und dessen Konzentration sinkt, wodurch der [[Calcium|Ca<sup>2+</sup>]]-Einstrom in die Nervenzelle sinkt und die Schmerzwahrnehmung abnimmt.<ref name="Udayakumar" /> Die Aktivierung von β-Arrestin ist vermutlich für die Atemdepression durch Opioide verantwortlich.<ref name="Comer" /> |
|||
Es hat aufgrund des hohen [[First-Pass-Effekt]]es eine perorale [[Bioverfügbarkeit]] von circa 30 %. Die Bioverfügbarkeit aus oral-transmukosalen oder transdermalen Darreichungsformen erreicht 50–90 %.<ref name="Lötsch">J. Lötsch, C. Walter, M. J. Parnham, B. G. Oertel, G. Geisslinger: ''Pharmacokinetics of non-intravenous formulations of fentanyl.'' In: ''[[Clinical Pharmacokinetics]].'' Band 52, Nummer 1, Januar 2013, S. 23–36, [[doi:10.1007/s40262-012-0016-7]], PMID 23100195.</ref> Fentanyl wirkt bei einer [[intravenös]]en Gabe nach fünf bis 120 Sekunden analgetisch.<ref>D. Häske und andere: ''Analgesie bei Traumapatienten in der Notfallmedizin.'' In: ''Der Anaesthesist'', Band 69, Nr. 2, Februar 2020, S. 137–148, hier: S. 141 (Wirkbeginn bei 0,6–2,5 µg/kgKG und intravenöser Gabe: 1–2 Minuten).</ref> Die maximale Wirkung tritt nach vier bis fünf Minuten ein. Die [[biologische Halbwertszeit]] liegt bei ein bis zwei Stunden.<ref>James M. Ritter, Rod Flower, Graeme Henderson, Yoon Kong Loke, David MacEwan, and Humphrey P. Rang: ''Rang & Dale's Pharmacology''. 9. Auflage 2020. Elsevier. ISBN 978-0-7020-7448-6. S. 556.</ref> Allgemein ist die Wirkung deutlich abhängig von der Dosis sowie Art und Dauer der Zufuhr (i.v.-Bolus oder kontinuierliche Zuführung etwa per Infusion).<ref name="mutsch" /> In der Anästhesiologie wurde der Begriff der [[Kontextsensitive Halbwertszeit|kontextsensitiven Halbwertszeit]] (CSHT) eingeführt, die angibt, nach welcher Zeit ab dem Stop einer kontinuierlichen Infusion der Plasmaspiegel auf die Hälfte abgesunken ist. Für Fentanyl nimmt die CSHT mit fortwährender Infusionsdauer stetig zu<ref name="schafer2016">M. Schäfer, C. Zöllner: ''Opioide in der Anästhesiologie''. In: Rossaint et al. (Hrsg.): ''Die Anästhesiologie''. Springer Reference Medizin. Springer, Berlin, Heidelberg. 2016. S. 1–24.</ref> und variiert mit der Größe des Eingriffs. Bei chirurgischen Patienten<ref>Fachinformation Fentanyl-Hexal 0,1 mg / 0,5 mg Injektionslösung, Stand März 2022. Hexal AG.</ref> wurde die Halbwertszeit mit 3 bis 12 Stunden<ref name="mutsch">G. Geisslinger et al.: ''Mutschler Arzneimittelwirkungen''. 11. Auflage. WVG, Stuttgart 2019, S. 304.</ref> bestimmt. Bei transdermaler Zufuhr führt auch noch nach Entfernen des Pflasters die kontinuierliche Abgabe von Fentanyl aus dem Hautdepot in den systemischen Kreislauf zu einer ungefähr 2- bis 3-mal längeren Halbwertzeit als nach intravenöser Gabe.<ref>Fachinformation Durogesic SMAT Transdermales Pflaster. Stand März 2022. Janssen-Cilag GmbH.</ref> Die Berechnung von Dosierungsschemata für in der Anästhesie intravenös verabreichte Opioide erfordert eine komplexere Berücksichtigung ihres pharmakokinetischen Verhaltens, welches in der Literatur mit Multikompartimentmodellen beschrieben wird.<ref name="gupta2011">D.K. Gupta, T.C. Krejcie, M.J. Avram: ''Pharmacokinetics of opioids''. In: ''Anesthetic Pharmacology'' (Hrsg.: A.S. Evers, M. Maze, E.D. Kharasch) Cambridge University Press, 2011. S. 509–530. [[doi:10.1017/cbo9780511781933.033]]</ref> Demnach fällt nach intravenöser Injektion die Fentanyl-Plasmakonzentration in drei Phasen unterschiedlich rasch ab, deren Halbwertszeiten rund 1 Minute, 19 Minuten und 7,9 Stunden betragen.<ref name="gupta2011" /> Die zur Behandlung effektive Dosis ([[Effektivdosis|ED<sub>50</sub>]]) liegt bei 2 bis 20 µg/kg Körpergewicht bei laufender Überwachung der Atmung. Die schmerzstillende Wirkdauer von Fentanyl ist abhängig von der angewendeten Arzneiform: 48 bis 72 Stunden bei einem transdermalen Pflaster, bei transmukosaler Applikation 0,5 bis 2 Stunden, bei Buccaltabletten und Sublingualtabletten 4 bis 6 Stunden.<ref name="Palliativmedizin. 2009">[[Eberhard Klaschik]]: ''Schmerztherapie und Symptomkontrolle in der Palliativmedizin.'' 2009, S. 233 f.</ref> Die analgetische Wirkdauer bei intravenöser Gabe von 0,6 bis 2,5 µg/kg beim spontan atmenden Patienten beträgt 20 bis 30 Minuten.<ref>D. Häske und andere: ''Analgesie bei Traumapatienten in der Notfallmedizin.'' In: ''Der Anaesthesist'', Band 69, Nr. 2, Februar 2020, S. 137–148, hier: S. 141.</ref> |
|||
| ⚫ | |||
Fentanyl wird hauptsächlich in der Leber verstoffwechselt und nur zu weniger als zehn Prozent unverändert über die [[Niere]]n ausgeschieden.<ref name="Comer" /> Der Hauptmetabolit Norfentanyl ist pharmakologisch inaktiv.<ref>Tom Peck and Benjamin Harris: ''Pharmacology for Anaesthesia and Intensive Care''. 5. Auflage 2021, Oxford University Press. ISBN 978-1-108-71096-1. [[doi:10.1017/9781108591317]]. S. 136.</ref> Weitere Metaboliten ergeben sich durch ''N''-Deacylierung, ''N''-Oxidierung und Hydroxylierung an aromatischen und aliphatischen Molekülpositionen.<ref name="pmid31024296">{{cite journal |author=Wilde M, Pichini S, Pacifici R, Tagliabracci A, Busardò FP, Auwärter V, Solimini R |title=Metabolic Pathways and Potencies of New Fentanyl Analogs |journal=Front Pharmacol |volume=10 |issue= |pages=238 |date=2019 |pmid=31024296 |pmc=6461066 |doi=10.3389/fphar.2019.00238 |url=}}</ref> Chronische Leber- oder Nierenerkrankungen haben nur einen geringen Einfluss auf den Abbau bzw. die Ausscheidung.<ref name="Ziesenitz">V. C. Ziesenitz, J. D. Vaughns, G. Koch, G. Mikus, J. N. van den Anker: ''Correction to: Pharmacokinetics of Fentanyl and Its Derivatives in Children: A Comprehensive Review.'' In: ''[[Clinical Pharmacokinetics]].'' Band 57, Nummer 3, März 2018, S. 393–417, [[doi:10.1007/s40262-017-0609-2]], PMID 29178007.</ref> |
|||
Die schmerzstillende Wirkdauer von Fentanyl ist abhängig von der angewendeten Arzneiform: 48 bis 72 Stunden bei einem transdermalen Pflaster, bei transmukosaler Applikation 0,5 bis 2 Stunden, bei Buccaltabletten und Sublingualtabletten 4 bis 6 Stunden.<ref name="Palliativmedizin. 2009" /> Die analgetische Wirkdauer bei intravenöser Gabe von 0,6 bis 2,5 µg/kg beim spontan atmenden Patienten beträgt 20 bis 30 Minuten.<ref>D. Häske und andere: ''Analgesie bei Traumapatienten in der Notfallmedizin.'' In: ''Der Anaesthesist'', Band 69, Nr. 2, Februar 2020, S. 137–148, hier: S. 141.</ref> Im Vergleich zu anderen Opioiden hat Fentanyl einen schnellen [[Wirkungseintritt]]<ref name="Kelly">E. Kelly, K. Sutcliffe, D. Cavallo, N. Ramos-Gonzalez, N. Alhosan, G. Henderson: ''The anomalous pharmacology of fentanyl.'' In: ''British journal of pharmacology.'' Mai 2021, [[doi:10.1111/bph.15573]], PMID 34030211.</ref> und ist relativ kurz wirkend.<ref name="Roewer" /> Es hat nach der Resorption aus hinuntergeschluckten oralen Formen aufgrund des hohen [[First-Pass-Effekt]]es eine [[Bioverfügbarkeit]] von circa 30 %. Der First-Pass-Effekt kann durch Gabe anderer nicht-intravenöser Formulierungen umgangen werden kann; so beträgt die Bioverfügbarkeit aus oral-transmukosalen oder transdermalen Darreichungsformen 50–90 %.<ref name="Lötsch">J. Lötsch, C. Walter, M. J. Parnham, B. G. Oertel, G. Geisslinger: ''Pharmacokinetics of non-intravenous formulations of fentanyl.'' In: ''[[Clinical Pharmacokinetics]].'' Band 52, Nummer 1, Januar 2013, S. 23–36, [[doi:10.1007/s40262-012-0016-7]], PMID 23100195.</ref> |
|||
Fentanyl hat eine polare Oberfläche von 23,6 [[Ångström (Einheit)|Å]]<sup>2</sup><!--Pubchem--> und ist mit einem [[Octanol-Wasser-Verteilungskoeffizient]]en von 717 sehr [[Lipophilie|lipophil]],<ref name="Lötsch" /> d. h. gut fettlöslich, und verteilt sich schnell in die Muskulatur und in fetthaltiges Gewebe. Dadurch kommt es zu einer Depotwirkung, die in einem [[Narkoseüberhang]] resultieren kann.<ref name="Roewer" /> Kelly ''et al.'' erklären die Potenz des Fentanyls mit einem die [[Zellmembran]] betreffenden Depot-Effekt. Sie zitieren Studien, die für Fentanyl [[Affinität (Biochemie)|Affinität]]en am MOR1 angeben, die etwas höher als die von Morphin sind, aber in der selben Größenordnung rangieren. Die hohe Lipophilie<!--cLogP = 4, gemäß pubchem--> des Moleküls führt zur Anreicherung des Stoffs in der Zellmembran und damit zur hohen Konzentration in der nahen Umgebung der Zielrezeptoren. [[Molekulardynamik-Simulation|Molekulardynamische Simulation]] legt nahe, dass der Wirkstoff mit seiner relativen Schlankheit und inneren Beweglichkeit aus der Ebene der Lipidschicht seitlich ins Rezeptorinnere vordringt und umgekehrt auch wieder rückdiffundiert. Ein derartiger Membran-Depot-Effekt erhöht die Ligandverfügbarkeit am Wirkort und kommt bei [[Hydrophilie|hydrophileren]] und starreren [[Morphinan]]-Opioiden wie Morphin (cLogP = 0,8)<!--pubchem--> nicht zur Geltung.<ref name="Kelly" /> |
|||
Fentanyl ist – wie auch sein [[Analogon (Chemie)|Analogon]] [[Sufentanil]] – sehr [[Lipophilie|lipophil]], d. h. mit einem [[Octanol-Wasser-Verteilungskoeffizient]]en von über 700<ref name="Lötsch" /> gut fettlöslich und verteilt sich schnell in die Muskulatur und in fetthaltiges Gewebe. Dadurch kommt es zu einer Depotwirkung, die in einem [[Narkoseüberhang]] resultieren kann.<ref name="Roewer" /> Allgemein ist die Wirkung deutlich abhängig von der Dosis sowie Art und Dauer der Zufuhr (i.v.-Bolus oder kontinuierliche Zuführung etwa per Infusion).<ref name="mutsch" /> In der Anästhesiologie wurde der Begriff der [[Kontextsensitive Halbwertszeit|kontextsensitiven Halbwertszeit]] (CSHT) eingeführt, die angibt, nach welcher Zeit ab dem Stop einer kontinuierlichen Infusion der Plasmaspiegel auf die Hälfte abgesunken ist. Für Fentanyl nimmt die CSHT mit fortwährender Infusionsdauer stetig zu<ref name="schafer2016">M. Schäfer, C. Zöllner: ''Opioide in der Anästhesiologie''. In: Rossaint et al. (Hrsg.): ''Die Anästhesiologie''. Springer Reference Medizin. Springer, Berlin, Heidelberg. 2016. S. 1–24.</ref> und variiert mit der Größe des Eingriffs. Bei chirurgischen Patienten<ref>Fachinformation Fentanyl-Hexal 0,1 mg / 0,5 mg Injektionslösung, Stand März 2022. Hexal AG.</ref> wurde die Halbwertszeit mit 3 bis 12 Stunden<ref name="mutsch">G. Geisslinger et al.: ''Mutschler Arzneimittelwirkungen''. 11. Auflage. WVG, Stuttgart 2019, S. 304.</ref> bestimmt. Bei transdermaler Zufuhr führt auch noch nach Entfernen des Pflasters die kontinuierliche Abgabe von Fentanyl aus dem Hautdepot in den systemischen Kreislauf zu einer ungefähr 2- bis 3-mal längeren Halbwertzeit als nach intravenöser Gabe.<ref>Fachinformation Durogesic SMAT Transdermales Pflaster. Stand März 2022. Janssen-Cilag GmbH.</ref> Fentanyl wird hauptsächlich in der [[Leber]] verstoffwechselt und nur zu weniger als zehn Prozent unverändert über die [[Niere]]n ausgeschieden.<ref name="Comer" /> In der Leber wird Fentanyl zum pharmakologisch inaktiven Norfentanyl ''N''-demethyliert (genauer: die Phenethylgruppe wird entfernt) und/oder hydroxyliert.<ref>Tom Peck and Benjamin Harris: ''Pharmacology for Anaesthesia and Intensive Care''. 5. Auflage 2021, Oxford University Press. ISBN 978-1-108-71096-1. [[doi:10.1017/9781108591317]]. S. 136.</ref> Chronische Leber- oder Nierenerkrankungen haben nur einen geringen Einfluss auf den Abbau bzw. die Ausscheidung.<ref name="Ziesenitz">V. C. Ziesenitz, J. D. Vaughns, G. Koch, G. Mikus, J. N. van den Anker: ''Correction to: Pharmacokinetics of Fentanyl and Its Derivatives in Children: A Comprehensive Review.'' In: ''[[Clinical Pharmacokinetics]].'' Band 57, Nummer 3, März 2018, S. 393–417, [[doi:10.1007/s40262-017-0609-2]], PMID 29178007.</ref> |
|||
| ⚫ | Fentanyl bindet aktivierend an [[Serotonin-Rezeptor]]en ([[Hemmkonstante|K<sub>i</sub>]] an 5HT<sub>1A</sub> 2,1 [[Molarität|μM]] und an 5HT<sub>2A</sub> 1,3 μM).<ref name="Baldo">B. A. Baldo, M. A. Rose: ''The anaesthetist, opioid analgesic drugs, and serotonin toxicity: a mechanistic and clinical review.'' In: ''British journal of anaesthesia.'' Band 124, Nummer 1, Januar 2020, S. 44–62, [[doi:10.1016/j.bja.2019.08.010]], PMID 31653394.</ref> Es ist ein schwacher Inhibitor des Serotonintransporters ([[SERT]]) mit einer [[IC50|IC<sub>50</sub>]] von 154 μM.<ref name="Baldo" /> Möglicherweise trägt die Aktivierung im Atemzentrum befindlicher Serotoninrezeptoren zur Letalität einer Überdosis bei.<ref name="Tao">R. Tao, M. Karnik, Z. Ma, S. B. Auerbach: ''Effect of fentanyl on 5-HT efflux involves both opioid and 5-HT1A receptors.'' In: ''British journal of pharmacology.'' Band 139, Nummer 8, August 2003, S. 1498–1504, [[doi:10.1038/sj.bjp.0705378]], PMID 12922937, {{PMC|1573976}}.</ref> Fentanyl hemmt [[HERG-Kanal|hERG1a/1b-Kanäle]] und fördert damit Herzrythmusstörungen.<ref name="pmid32321735">{{cite journal |author=Tschirhart JN, Zhang S |title=Fentanyl-Induced Block of hERG Channels Is Exacerbated by Hypoxia, Hypokalemia, Alkalosis, and the Presence of hERG1b |journal=Mol Pharmacol |volume=98 |issue=4 |pages=508–517 |date=2020 |pmid=32321735 |doi=10.1124/mol.119.119271 |url=}}</ref> |
||
Die Struktur des MOR1 mit gebundenem Fentanyl wurde [[elektronenmikroskop]]isch bestimmt ({{PDB2|8EF5}}) und im Jahr 2022 veröffentlicht.<ref>Y. Zhuang, Y. Wang, B. He, et al.: ''Molecular recognition of morphine and fentanyl by the human μ-opioid receptor.'' In: ''[[Cell (Zeitschrift)|Cell]].'' Band 185, Nummer 23, November 2022, S. 4361–4375.e19, [[doi:10.1016/j.cell.2022.09.041]], PMID 36368306.</ref> Molekulardynamische Simulation legt nahe, das Fentanyl an der orthosterischen MOR1-Bindungsstelle mindestens zwei Lagen sowie mehrere [[Konformation]]en einnehmen kann.<ref name="Kelly" /> |
|||
Es gibt Hinweise, dass Fentanyl eine geringe [[Kreuztoleranz]] hat gegenüber Morphinan-Opioiden wie etwa Heroin. Es besteht aber Bedarf an einer systematischeren Prüfung.<ref name="Kelly" /> |
|||
== Synthese == |
== Synthese == |
||
=== Janssen-Methode === |
=== Janssen-Methode === |
||
Gemäß der von Paul Janssen ursprünglich entwickelten<!-- Das Patent von 1964 beschreibt nur den letzten Syntheseschritt. --> und aus heutiger Sicht als umständlich geltenden Synthese wird 4-Piperidinon zunächst per ''N''-[[Benzylgruppe|Benzylierung]] [[Schutzgruppe|geschützt]]. Das anschließend durch [[Kondensationsreaktion|Kondensation]] des Ketons NPP mit Anilin entstehende [[Imin]] wird mit [[Lithiumaluminiumhydrid]] reduziert. Das so erhaltene 4-ANPP wird mit [[ |
Gemäß der von Paul Janssen ursprünglich entwickelten<!-- Das Patent von 1964 beschreibt nur den letzten Syntheseschritt. --> und aus heutiger Sicht als umständlich geltenden Synthese wird 4-Piperidinon zunächst per ''N''-[[Benzylgruppe|Benzylierung]] [[Schutzgruppe|geschützt]]. Das anschließend durch [[Kondensationsreaktion|Kondensation]] des Ketons NPP mit Anilin entstehende [[Imin]] wird mit [[Lithiumaluminiumhydrid]] reduziert. Das so erhaltene 4-ANPP wird mit [[Propionsäureanhydrid]] zum Benzylfentanyl ''N''-[[Acylierung|acycliert]]. Das durch [[Hydrogenolyse|hydrogenolytische]] Debenzylierung entstehende Norfentanyl wird mit Phenethylchlorid ''N''-alkyliert, so dass sich Fentanyl als Endprodukt ergibt.<ref>{{Cite web |date=2020-06-18 |title=Fentanyl Synthesis |url=https://gpatindia.com/fentanyl-synthesis-sar-mcqstructurechemical-properties-and-therapeutic-uses/ |url-status=live |archive-url=https://archive.ph/TmrEi |archive-date=2022-12-28 |website=GPTA India}}</ref> |
||
=== Siegfried-Methode und Valdez-Variante === |
=== Siegfried-Methode und Valdez-Variante === |
||
[[Datei:NPP to fentanyl.svg|mini|Siegfried-Methode]] |
[[Datei:NPP to fentanyl.svg|mini|Siegfried-Methode]] |
||
Die „Siegfried“-Route, die ihren Ursprung in einer privaten, von [[Erowid]] archivierten Internet-Veröffentlichung hat, verzichtet auf das aufwändige Schutzgruppenkonzept, indem sie die ''N''-Alkylierung in den ersten Syntheseschritt verlegt. Das resultierende NNP wird mit Anilin zum Imin kondensiert, welches zu 4-ANPP reduziert wird. Die herkömmliche |
Die „Siegfried“-Route, die ihren Ursprung in einer privaten, von [[Erowid]] archivierten Internet-Veröffentlichung hat, verzichtet auf das aufwändige Schutzgruppenkonzept, indem sie die ''N''-Alkylierung in den ersten Syntheseschritt verlegt. Das resultierende NNP wird mit Anilin zum Imin kondensiert, welches zu 4-ANPP reduziert wird. Die herkömmliche Propionylierung ergibt das Endprodukt in einer Gesamtausbeute von 50 bis 80 %.<ref>Siegfried, ''[https://www.erowid.org/archive/rhodium/chemistry/fentanyl.html Synthesis of Fentanyl]'', Erowid-Archiv.</ref> In verschiedenen Ländern machten klandestin Fentanyl produzierende Labore in den frühen 2000er Jahren Gebrauch vom Siegfried-Verfahren.<ref>{{cite web |title=Designation of Benzylfentanyl and 4-Anilinopiperidine, Precursor Chemicals Used in the Illicit Manufacture of Fentanyl, as List I Chemicals |url=https://www.federalregister.gov/documents/2020/04/15/2020-07064/designation-of-benzylfentanyl-and-4-anilinopiperidine-precursor-chemicals-used-in-the-illicit |website=federalregister.gov |publisher=[[Drug Enforcement Administration|DEA]] |access-date=2023-01-28 |date=2020-04-15}}</ref> Eine ausbeutenoptimierte Variante, die einen [[Reduktive Aminierung|reduktiven Aminierungsschritt]] enthält, stellten Valdez et al. im Jahr 2014 vor.<ref>Valdez CA, Leif RN, Mayer BP (2014): ''[https://journals.plos.org/plosone/article?id=10.1371/journal.pone.0108250 An Efficient, Optimized Synthesis of Fentanyl and Related Analogs]''. Plos One.</ref> |
||
=== Gupta-Methode === |
=== Gupta-Methode === |
||
[[Datei:GuptaFent2.jpg|mini|Gupta-Methode]] |
[[Datei:GuptaFent2.jpg|mini|Gupta-Methode]] |
||
Ein [[Eintopfreaktion|Eintopfverfahren]] aus dem Jahr 2005 folgt einer reduktiven [[Tandem-Reaktion|Tandem]]-Aminierung, die [[Natriumtriacetoxyborhydrid]] (NTAB) als Reagenz verwendet. Dabei reagiert [[Phenylethanal|Phenylacetaldehyd]] mit 4-Piperidinon zu NPP, und zwar [[Chemoselektivität|chemoselektiv]], da der Aldehyd die reaktivere [[Carbonyl]]komponente ist. Das Keton reagiert anschließend mit Anilin ''[[in situ]]'' zum 4-ANPP. Die abschließende ''N''-Propionylierung erfordert ebenfalls keine Isolation des Ansatzes, da das überschüssige NTAB als Abfangreagenz genügt.<ref>Gupta PK, Ganesan K, Pande A, Malhotra RC (2005): ''[https://journals.sagepub.com/doi/pdf/10.3184/030823405774309078 A convenient one pot synthesis of fentanyl]''. J. Chem. Res., S. 452, </ref> Ausbeuten bis zu 81 %<ref>Asadi Z, et al. (2017): ''[https://www.sciencedirect.com/science/article/abs/pii/S0022286016309541 A structural study of fentanyl by DFT calculations, NMR and IR spectroscopy]''. [[J. Mol. Struct.]], S. 552.</ref> und leichte Durchführbarkeit machen dieses Verfahren für eine ökonomische Massenproduktion attraktiv. Entsprechend ist das Gupta-Verfahren in der illegalen Fentanyl-Produktion der Gegenwart vorherrschend, wie sich im Jahr 2021 auf Grundlage einer [[Chemisches Profiling|Profiling-Analyse]] herausstellte, welche 318 in den Vereinigten Staaten beschlagnahmte fentanylhaltige Drogenpräparate untersuchte. Der durchschnittliche Fentanylanteil der Proben betrug 13,6 %, die Spanne reichte von 0,2 % bis 36,4 %. Ein hoher Anteil herkömmlicher Streckstoffe wurde dabei identifiziert.<ref>{{cite web |title=Fentanyl Profiling Program Report |url=https://www.dea.gov/sites/default/files/2022-05/FPP%20Report%20January%202022.pdf | work = Special Testing and Research Laboratory | publisher = Drug Enforcement Administration |access-date=2023-01-25 |page=1–2}}</ref> |
Ein [[Eintopfreaktion|Eintopfverfahren]] aus dem Jahr 2005 folgt einer reduktiven [[Tandem-Reaktion|Tandem]]-Aminierung, die [[Natriumtriacetoxyborhydrid]] (NTAB) als Reagenz verwendet. Dabei reagiert [[Phenylethanal|Phenylacetaldehyd]] mit 4-Piperidinon zu NPP, und zwar [[Chemoselektivität|chemoselektiv]], da der Aldehyd die reaktivere [[Carbonyl]]komponente ist. Das Keton reagiert anschließend mit Anilin ''[[in situ]]'' zum 4-ANPP. Die abschließende ''N''-Propionylierung erfordert ebenfalls keine Isolation des Ansatzes, da das überschüssige NTAB als Abfangreagenz genügt.<ref>Gupta PK, Ganesan K, Pande A, Malhotra RC (2005): ''[https://journals.sagepub.com/doi/pdf/10.3184/030823405774309078 A convenient one pot synthesis of fentanyl]''. J. Chem. Res., S. 452, </ref> Ausbeuten bis zu 81 %<ref>Asadi Z, et al. (2017): ''[https://www.sciencedirect.com/science/article/abs/pii/S0022286016309541 A structural study of fentanyl by DFT calculations, NMR and IR spectroscopy]''. [[J. Mol. Struct.]], S. 552.</ref> und leichte Durchführbarkeit machen dieses Verfahren für eine ökonomische Massenproduktion attraktiv. Entsprechend ist das Gupta-Verfahren in der illegalen Fentanyl-Produktion der Gegenwart vorherrschend, wie sich im Jahr 2021 auf Grundlage einer [[Chemisches Profiling|Profiling-Analyse]] herausstellte, welche 318 in den Vereinigten Staaten beschlagnahmte fentanylhaltige Drogenpräparate untersuchte. Der durchschnittliche Fentanylanteil der Proben betrug 13,6 %, die Spanne reichte von 0,2 % bis 36,4 %. Ein hoher Anteil herkömmlicher Streckstoffe wurde dabei identifiziert.<ref>{{cite web |title=Fentanyl Profiling Program Report |url=https://www.dea.gov/sites/default/files/2022-05/FPP%20Report%20January%202022.pdf | work = Special Testing and Research Laboratory | publisher = Drug Enforcement Administration |access-date=2023-01-25 |page=1–2}}</ref> |
||
<!-- |
|||
Für weitere Verfahren auf Relevanzkriterien und eine sinnvolle Beschreibung achten. |
|||
--> |
|||
== Analytik == |
== Analytik == |
||
Version vom 16. September 2023, 13:42 Uhr
| Strukturformel | ||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|

| ||||||||||||||||||||||
| Allgemeines | ||||||||||||||||||||||
| Freiname | Fentanyl[1] | |||||||||||||||||||||
| Andere Namen | ||||||||||||||||||||||
| Summenformel | C22H28N2O | |||||||||||||||||||||
| Kurzbeschreibung |
Weißes bis fast weißes, polymorphes Pulver[2] | |||||||||||||||||||||
| Externe Identifikatoren/Datenbanken | ||||||||||||||||||||||
| ||||||||||||||||||||||
| Arzneistoffangaben | ||||||||||||||||||||||
| ATC-Code | ||||||||||||||||||||||
| Wirkstoffklasse | ||||||||||||||||||||||
| Eigenschaften | ||||||||||||||||||||||
| Molare Masse | 336,47 g·mol−1 | |||||||||||||||||||||
| Schmelzpunkt | ||||||||||||||||||||||
| Löslichkeit | ||||||||||||||||||||||
| Sicherheitshinweise | ||||||||||||||||||||||
| ||||||||||||||||||||||
| Toxikologische Daten | ||||||||||||||||||||||
| Soweit möglich und gebräuchlich, werden SI-Einheiten verwendet. Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen (0 °C, 1000 hPa). | ||||||||||||||||||||||
Fentanyl (auch Fentanil) ist ein synthetisches Opioid, das als Schmerzmittel (Analgetikum) in der Anästhesie (bei Narkosen) sowie zur Therapie akuter und chronischer Schmerzen, die nur mit Opioidanalgetika ausreichend behandelt werden können, eingesetzt wird. Es wird als Injektion, transdermales Pflaster, oral-transmukosale Zubereitung und als Nasenspray verwendet und gilt als unentbehrliches Arzneimittel der WHO.[10]
Fentanyl wirkt als Agonist am μ-Opioidrezeptor.[11] Fentanyl ist als Arznei- und Rauschmittel unter anderem dem deutschen und Schweizer Betäubungsmittelgesetz sowie dem österreichischen Suchtmittelgesetz unterstellt. In den Vereinigten Staaten ist Fentanyl das Arznei- oder Rauschmittel, das wegen illegaler Nutzung 2021 zu den meisten Überdosis-Toten geführt hat (Opioidkrise in den Vereinigten Staaten).[12]
Geschichte

Fentanyl wurde in den frühen 1960ern von Paul Janssen als erstes Anilinopiperidin entwickelt.[13][14] Es gehört zur größeren Gruppe der Pethidin-abgeleiteten Opioide[15] und wurde bei der Untersuchung der Wirkungen von Pethidin-Analoga entdeckt.[16] Fentanyl wird als Citrat verwendet[17] und wurde als Medikament 1963 in einigen westeuropäischen Ländern eingeführt.[14] In den Vereinigten Staaten wurde es 1968 unter dem Handelsnamen Sublimaze zugelassen.[18][19] Seitdem wurden aus Fentanyl durch Modifikationen der Molekülstruktur eine Reihe besser steuerbarer Analoga und Derivate entwickelt.[13][20][21] Es werden Fentanyl-Derivate untersucht, die zur Verstärkung der Wirkung eine zweite Funktion zur Bindung an andere schmerzassoziierte Rezeptoren aufweisen.[21][22]
Auch bei den Darreichungsformen gab es Entwicklungen. In den 1990er Jahren wurden Fentanylpflaster für die Zufuhr des Wirkstoffs durch die Haut entwickelt.[23] Im Jahr 1998 wurden Fentanyllutschtabletten zugelassen,[24] ab 2009 folgten wasserlösliche Fentanylschmelzfilme[25] als Formulierungen für die Resorption über die Mundschleimhaut. Jüngere Formulierungen solcher Rapid-Onset Opioids (ROOs) ermöglichen die Applikation von Fentanyl über die Nase (Nasenspray).[14] Der Großteil medizinisch verwendeten Fentanyls wird in Europa und den Vereinigten Staaten eingesetzt (insgesamt 75 % des Weltmarktes in 2020), darunter in den Vereinigten Staaten und Deutschland mit je etwa 18 % des Weltmarkts von 2018–2020.[26] Die Herstellung von medizinisch verwendetem Fentanyl (Administrative Controlled Substances Code Number 9801) nahm von 2300 kg im Jahr 2016 auf 731 kg im Jahr 2021 ab.[27]
Seit 1979 wird Fentanyl nichtmedizinisch (illegalerweise) verwendet,[28] seit den 2000er Jahren zunehmend und insbesondere in Nordamerika, der EU und Großbritannien.[29] In den letzten Jahren ist eine Reihe von Fentanyl-Derivaten für den Schwarzmarkt entwickelt worden.[30] Der größte Markt für nichtmedizinisch verwendetes Fentanyl sind die Vereinigten Staaten. Der Großteil wurde ab 2013 in China hergestellt. Da seit 2019 in China die Herstellung und Anwendung von Fentanyl kontrolliert wird, werden für nichtmedizinisch verwendetes Fentanyl zunehmend die Vorläuferstoffe für die Synthese von Fentanyl von China nach Mexiko geliefert, wo es für den nordamerikanischen Schwarzmarkt hergestellt wird.[29]
Wirkung
Fentanyl wirkt stark schmerzlindernd (analgetisch) und sedierend, daneben auch atemdepressiv, antitussiv, pulsverlangsamend, blutdrucksenkend, verstopfend und teils euphorisierend.[31] Der Konsum von Fentanyl aktiviert das Belohnungssystem und wirkt verstärkend, was hauptursächlich zum Missbrauch und zu Todesfällen durch Überdosierung beiträgt.[32] Im Vergleich zu anderen Opioiden verursacht Fentanyl eine stärkere Muskelsteifheit.[32]
Anwendungsgebiete
Fentanyl wird unter anderem in der Anästhesie,[33] Onkologie,[34][35] Militärmedizin,[36] Palliativmedizin[37] und Geburtsheilkunde[38][39] als Schmerzmittel eingesetzt.
In der Anästhesie wird es zur Narkose,[33] zur Spinal-[40] und zur Epiduralanästhesie[39] verwendet. Fentanyl ist das meistverwendete Opioid-Anästhetikum für Analgesie während einer Operation, unter anderem weil es wenige kardiovaskuläre Effekte und wenig Histaminausschüttung hervorruft.[41] Haupteinsatzgebiet der intravenösen Form ist die Gabe als Schmerzmittel bei Operationen in Verbindung mit einem Schlafmittel und wahlweise einem muskelentspannenden Mittel (Muskelrelaxans). Je nach Wahl des Schlafmittels spricht man von „balancierter Anästhesie“ oder „totaler intravenöser Anästhesie“ (TIVA). Wegen der Gefahr der Atemdepression ist eine ständige Überwachung und das Bereithalten einer Beatmungsmöglichkeit erforderlich. Aufgrund der Lipophilie wird Fentanyl teilweise schwer kontrollierbar im Fettgewebe eingelagert und wieder freigegeben. Deshalb werden heute anstelle von Fentanyl häufig die weniger lipophilen verwandten Stoffe Alfentanil und Remifentanil verwendet. Bei fentanylhaltigen Wirkstoffpflastern ist wegen der gleichmäßigen Wirkung und der im Vergleich zur Anästhesie meist deutlich geringeren Dosis nach einer Einstellungsphase keine ständige Überwachung der Vitalfunktionen nötig.
Anwendungsformen
Gebräuchlich ist Fentanyl als Fentanyldihydrogencitrat. Es gibt vier Anwendungsformen:
- als Injektion (etwa in der Anästhesie oder Notfallmedizin);
- als transdermales therapeutisches System (d. h. als auf die Haut geklebtes Membranpflaster bzw. Matrixpflaster), das den Wirkstoff (mit wahlweise 12,5, 25, 37,5, 50, 75, 100 oder 150 Mikrogramm pro Stunde) zur Aufnahme über die Haut freisetzt; teilweise auch per Iontophorese[42]
- als schnell freisetzende Formulierung für die Aufnahme über die Mundschleimhäute (oral-transmukosal), etwa als 200 bis 1600 µg Wirkstoff enthaltende Lutschtablette mit integriertem Applikator zur Anwendung an der Mundschleimhaut, als Buccaltablette mit 100 bis 800 µg Wirkstoff oder als Sublingualtablette mit 50 bis 800 µg Fentanyl;
- die nasale Applikation, als Fentanyl-Nasenspray.
Diese schnell freisetzenden Formulierungen sind indiziert für die Behandlung von Durchbruchschmerzen (sehr intensiver minutenlanger Schmerz, typisch bei fortgeschrittener Krebserkrankung) bei Erwachsenen, die bereits eine Opioid-Basistherapie gegen ihre Tumorschmerzen erhalten.[43]
-
Ein transdermales Pflaster mit einer Freisetzungsrate von 12 Mikrogramm Fentanyl pro Stunde am Arm einer Person
-
Lutschtablette (400 Mikrogramm Fentanyl) mit Applikator
Nebenwirkungen
Wie auch andere Opioide provoziert Fentanyl bei Überdosierung eine Störung des Zentralnervensystems mit Bewusstseinsstörungen, Somnolenz und Atemdepression.[44] Das akute Bild weist im Wesentlichen ausgeprägte Sedierung, Miosis (Verengung der Pupille) und Atemdepression auf, wobei diese bis hin zum Atemstillstand besonders hervorzuheben ist. Fentanyl kann mit Naloxon antagonisiert werden.
Typische Nebenwirkungen umfassen Übelkeit, Erbrechen, Verstopfung, Jucken, Benommenheit, Verwirrtheit und Verletzungen durch mangelhafte Koordination.[45][46] Schwerwiegende Nebenwirkungen umfassen Atemdepression, Sinnestäuschungen, Serotonin-Syndrom, niedriger Blutdruck und Opiatabhängigkeit.[45][46] Im Vergleich zu Morphin erzeugt Fentanyl weniger Juckreiz und weniger Übelkeit.[47] Die Muskelsteifheit in Brustkorb und Abdomen ist bei Fentanyl relativ stark ausgeprägt, was als wooden chest syndrome (‚hölzerner-Brustkorb-Syndrom‘) bezeichnet wird[48] und vermutlich durch die Ausschüttung von Noradrenalin und Acetylcholin verursacht wird.[49] Die Muskelsteifheit in den Muskeln der Atemwege kann eine Beatmung mit Beatmungsbeutel erschweren.[44] Fentanyl erzeugt eine Bradykardie (Absenkung der Herzschlagfrequenz) durch eine Aktivierung des Parasympathikus in Folge einer Aktivierung des Vagusnervs.[44] Daneben wirkt Fentanyl gefäßerweiternd, wodurch der Blutdruck sinkt.[44] Die Gefäßweitung basiert zum überwiegenden Teil auf einer Wirkung im Gehirn, zum geringeren Teil durch direkte Einwirkung auf die Gefäße.[44] Der Effekt der Gefäßweitung ist besonders ausgeprägt in Patienten mit Bluthochdruck oder Herz-Kreislauferkrankungen.[44]
Anwendungssicherheit
In einem Rote-Hand-Brief warnten Hersteller von Fentanylpflastern 2014 vor einer versehentlichen Übertragung des Fentanylpflasters auf die Haut einer anderen Person, z. B. während der gemeinsamen Nutzung eines Bettes oder beim engeren Körperkontakt. „Zum Schutz gegen versehentliches Verschlucken durch Kinder soll die Applikationsstelle sorgfältig ausgewählt und regelmäßig überwacht werden, ob sich das Pflaster noch dort befindet.“[50]
Seit in den Vereinigten Staaten – allein bis 2012 über zehn[51] – Kinder nach Kontakt mit Fentanylpflastern an einer Überdosis verstarben, warnt die FDA Eltern und Betreuer vor den tödlichen Gefahren der versehentlichen Exposition und betont die Notwendigkeit eines verantwortungsbewussten Umgangs mit den Pflastern. Sie veröffentlicht Tipps für Vorsichtsmaßnahmen und empfiehlt, mit dem Arzt das Vorhalten von Naloxon als Gegenmittel zu besprechen.[52] Im März 2023 erfolgte in den USA die Zulassung eines rezeptfreien Naloxon-Nasensprays als Gegenmittel bei Opioid-Überdosierungen;[53] zuvor schon hatte sich die FDA für eine Entlassung aus der Rezeptpflicht ausgesprochen.[54]
Die Koordinierungsgruppe (CMDh) der nationalen Arzneimittelbehörden der EU beschloss im Dezember 2022, dass umfassende Maßnahmen getroffen werden sollen, um die Anwendungssicherheit von Fentanyl-Arzneimitteln zu erhöhen. Unter anderem müssen Hersteller die Verpackungen von Fentanylpflastern mit dem Warnhinweis „Versehentliche Anwendung oder Einnahme kann tödlich sein“ beschriften. Vorangegangen waren schwerwiegende Zwischenfälle durch versehentliche Exposition und Überdosierung. Patienten und Pflegekräfte sind anzuweisen, die Präparate vor dem Zugriff durch andere zu schützen.[55]
Nachdem es in den USA Presseberichten zufolge bei Helfern vor Ort zu Vergiftungen durch unbeabsichtigten Kontakt mit Fentanyl gekommen sein soll, entkräftete eine Studie diese Möglichkeit der Intoxikation. Eine Aufnahme giftiger Mengen von Fentanylpulver über die Haut sei sehr unwahrscheinlich.[56]
Seit 2005 berichtet die Food and Drug Administration (FDA) wiederholt über schwere Nebenwirkungen und Todesfälle in Zusammenhang mit fentanylhaltigen transdermalen therapeutischen Systemen, allein 2009 über 397 Todesfälle.[57][58] So verwies auch die Arzneimittelkommission der deutschen Ärzteschaft (AkdÄ) 2012 darauf, dass die Indikation für transdermale, fentanylhaltige Pflaster streng zu stellen ist. So sollen sie nur bei chronischen Schmerzen verordnet werden, die nur mit Opioiden ausreichend gelindert werden und einer andauernden, kontinuierlichen Behandlung bedürfen. Während die FDA die Anwendung nur bei Patienten erlaubt, die über mindestens eine Woche 60 mg Morphin pro Tag oder mehr eingenommen haben (oder entsprechend ein anderes Opioid), rät die deutsche Fachinformation, bei Patienten ohne bisherige Opioideinnahme zunächst niedrig dosiert unretardierte Opioide zu geben, bis deren Dosis 12,5 μg/h Fentanyl (= 45 mg Morphin/Tag) entspricht, und erst dann auf ein Pflaster umzustellen.[59]
Wechselwirkungen
Die sedierende Wirkung von Fentanyl kann durch Beruhigungsmittel und Alkohol verstärkt werden. In Verbindung mit Monoaminooxidase-Hemmern können schwere Kreislauf- und Atemstörungen auftreten. Zwischen der Anwendung von MAO-Hemmern und Fentanyl sollen mindestens 14 Tage liegen. Durch die Plasmaeiweißbindung von 90 % kann es bei Verwendung in Schmerzpflastern zu Wechselwirkungen mit Präparaten wie Furosemid, Glibenclamid oder Omeprazol kommen. Der Abbauweg von Fentanyl führt über die Cytochromoxidase 450,[60] so dass bei gleichzeitiger Einnahme von CYP 3A4-Induktoren (z. B. Johanniskraut-Präparate; beschleunigen den Abbau von Fentanyl) oder CYP 3A4-Inhibitoren (z. B. Ketoconazol, Erythromycin, Nefazodon, Diltiazem, Grapefruitsaft; verlangsamen den Abbau von Fentanyl und können zu erhöhten Plasmaspiegeln führen) Wechselwirkungen auftreten können.
Die Kombination von Fentanyl (und anderen Opioiden) mit Calciumantagonisten kann neben der Verminderung der Toleranzentwicklung auch zu einer Potenzierung der analgetischen Wirkung führen. 1985 wurde die potenzierende Wirkung von Nimodipin gegenüber der analgetischen Wirkung von Fentanyl beschrieben. So soll die kombinierte Gabe von 0,1 mg Fentanyl zusammen mit Nimodipin (1 µg/kg/min Infusion) die gleiche Wirksamkeit wie 2,45 mg Fentanyl besitzen, was einer Potenzierung um das 24,5-fache entspricht.[61] Weitere Humanversuche zeigten, dass Nifedipin im Gegensatz zu Nimodipin keine Potenzierung der Fentanyl-Wirkung verursacht, allerdings war auch der Effekt von Nimodipin in dieser Studie deutlich schwächer (3-fache Potenzierung), als in der ersten Studie.[62]
Durch die gleichzeitige Gabe von fentanylhaltigen Arzneimitteln mit serotonerg wirkenden Arzneimitteln (SSRI/SNRI) besteht ein Risiko für das Auftreten eines gefährlichen Serotoninsyndroms mit Symptomen wie Agitiertheit, Koma, Halluzinationen, Blutdruckkrisen, neuromuskulären Veränderungen und Herzrasen, wie im März 2013 gewarnt wurde.[63]
Pharmakologie
| Affinitäten, Ki | Verhältnis | ||
|---|---|---|---|
| μ-Opioid- Rezeptor (MOR) |
δ-Opioid- Rezeptor (DOR) |
κ-Opioid- Rezeptor (KOR) |
MOR:DOR:KOR |
| 0,39 nM | >1.000 nM | 255 nM | 1:>2564:654 |
Fentanyl erzeugt seine analgetische Wirkung wie auch viele seiner Nebenwirkungen durch Aktivierung des μ-Opioidrezeptors (MOR). Fentanyl ist etwa 50 bis 100 mal so potent wie Morphin, was bedeutet, dass Fentanyl mit einem Hundertstel der Masse von Morphin die gleiche Intensität der Schmerzlinderung erreicht. Im Vergleich zu vielen anderen Opioiden hat Fentanyl einen schnellen Wirkungseintritt[65] und eine relativ kurze Wirkungsdauer.[11]
Es hat aufgrund des hohen First-Pass-Effektes eine perorale Bioverfügbarkeit von circa 30 %. Die Bioverfügbarkeit aus oral-transmukosalen oder transdermalen Darreichungsformen erreicht 50–90 %.[66] Fentanyl wirkt bei einer intravenösen Gabe nach fünf bis 120 Sekunden analgetisch.[67] Die maximale Wirkung tritt nach vier bis fünf Minuten ein. Die biologische Halbwertszeit liegt bei ein bis zwei Stunden.[68] Allgemein ist die Wirkung deutlich abhängig von der Dosis sowie Art und Dauer der Zufuhr (i.v.-Bolus oder kontinuierliche Zuführung etwa per Infusion).[69] In der Anästhesiologie wurde der Begriff der kontextsensitiven Halbwertszeit (CSHT) eingeführt, die angibt, nach welcher Zeit ab dem Stop einer kontinuierlichen Infusion der Plasmaspiegel auf die Hälfte abgesunken ist. Für Fentanyl nimmt die CSHT mit fortwährender Infusionsdauer stetig zu[70] und variiert mit der Größe des Eingriffs. Bei chirurgischen Patienten[71] wurde die Halbwertszeit mit 3 bis 12 Stunden[69] bestimmt. Bei transdermaler Zufuhr führt auch noch nach Entfernen des Pflasters die kontinuierliche Abgabe von Fentanyl aus dem Hautdepot in den systemischen Kreislauf zu einer ungefähr 2- bis 3-mal längeren Halbwertzeit als nach intravenöser Gabe.[72] Die Berechnung von Dosierungsschemata für in der Anästhesie intravenös verabreichte Opioide erfordert eine komplexere Berücksichtigung ihres pharmakokinetischen Verhaltens, welches in der Literatur mit Multikompartimentmodellen beschrieben wird.[73] Demnach fällt nach intravenöser Injektion die Fentanyl-Plasmakonzentration in drei Phasen unterschiedlich rasch ab, deren Halbwertszeiten rund 1 Minute, 19 Minuten und 7,9 Stunden betragen.[73] Die zur Behandlung effektive Dosis (ED50) liegt bei 2 bis 20 µg/kg Körpergewicht bei laufender Überwachung der Atmung. Die schmerzstillende Wirkdauer von Fentanyl ist abhängig von der angewendeten Arzneiform: 48 bis 72 Stunden bei einem transdermalen Pflaster, bei transmukosaler Applikation 0,5 bis 2 Stunden, bei Buccaltabletten und Sublingualtabletten 4 bis 6 Stunden.[74] Die analgetische Wirkdauer bei intravenöser Gabe von 0,6 bis 2,5 µg/kg beim spontan atmenden Patienten beträgt 20 bis 30 Minuten.[75]
Fentanyl wird hauptsächlich in der Leber verstoffwechselt und nur zu weniger als zehn Prozent unverändert über die Nieren ausgeschieden.[76] Der Hauptmetabolit Norfentanyl ist pharmakologisch inaktiv.[77] Weitere Metaboliten ergeben sich durch N-Deacylierung, N-Oxidierung und Hydroxylierung an aromatischen und aliphatischen Molekülpositionen.[78] Chronische Leber- oder Nierenerkrankungen haben nur einen geringen Einfluss auf den Abbau bzw. die Ausscheidung.[79]
Fentanyl hat eine polare Oberfläche von 23,6 Å2 und ist mit einem Octanol-Wasser-Verteilungskoeffizienten von 717 sehr lipophil,[66] d. h. gut fettlöslich, und verteilt sich schnell in die Muskulatur und in fetthaltiges Gewebe. Dadurch kommt es zu einer Depotwirkung, die in einem Narkoseüberhang resultieren kann.[11] Kelly et al. erklären die Potenz des Fentanyls mit einem die Zellmembran betreffenden Depot-Effekt. Sie zitieren Studien, die für Fentanyl Affinitäten am MOR1 angeben, die etwas höher als die von Morphin sind, aber in der selben Größenordnung rangieren. Die hohe Lipophilie des Moleküls führt zur Anreicherung des Stoffs in der Zellmembran und damit zur hohen Konzentration in der nahen Umgebung der Zielrezeptoren. Molekulardynamische Simulation legt nahe, dass der Wirkstoff mit seiner relativen Schlankheit und inneren Beweglichkeit aus der Ebene der Lipidschicht seitlich ins Rezeptorinnere vordringt und umgekehrt auch wieder rückdiffundiert. Ein derartiger Membran-Depot-Effekt erhöht die Ligandverfügbarkeit am Wirkort und kommt bei hydrophileren und starreren Morphinan-Opioiden wie Morphin (cLogP = 0,8) nicht zur Geltung.[65]
Fentanyl bindet aktivierend an Serotonin-Rezeptoren (Ki an 5HT1A 2,1 μM und an 5HT2A 1,3 μM).[41] Es ist ein schwacher Inhibitor des Serotonintransporters (SERT) mit einer IC50 von 154 μM.[41] Möglicherweise trägt die Aktivierung im Atemzentrum befindlicher Serotoninrezeptoren zur Letalität einer Überdosis bei.[80] Fentanyl hemmt hERG1a/1b-Kanäle und fördert damit Herzrythmusstörungen.[81]
Die Struktur des MOR1 mit gebundenem Fentanyl wurde elektronenmikroskopisch bestimmt (8EF5) und im Jahr 2022 veröffentlicht.[82] Molekulardynamische Simulation legt nahe, das Fentanyl an der orthosterischen MOR1-Bindungsstelle mindestens zwei Lagen sowie mehrere Konformationen einnehmen kann.[65]
Es gibt Hinweise, dass Fentanyl eine geringe Kreuztoleranz hat gegenüber Morphinan-Opioiden wie etwa Heroin. Es besteht aber Bedarf an einer systematischeren Prüfung.[65]
Synthese
Janssen-Methode
Gemäß der von Paul Janssen ursprünglich entwickelten und aus heutiger Sicht als umständlich geltenden Synthese wird 4-Piperidinon zunächst per N-Benzylierung geschützt. Das anschließend durch Kondensation des Ketons NPP mit Anilin entstehende Imin wird mit Lithiumaluminiumhydrid reduziert. Das so erhaltene 4-ANPP wird mit Propionsäureanhydrid zum Benzylfentanyl N-acycliert. Das durch hydrogenolytische Debenzylierung entstehende Norfentanyl wird mit Phenethylchlorid N-alkyliert, so dass sich Fentanyl als Endprodukt ergibt.[83]
Siegfried-Methode und Valdez-Variante

Die „Siegfried“-Route, die ihren Ursprung in einer privaten, von Erowid archivierten Internet-Veröffentlichung hat, verzichtet auf das aufwändige Schutzgruppenkonzept, indem sie die N-Alkylierung in den ersten Syntheseschritt verlegt. Das resultierende NNP wird mit Anilin zum Imin kondensiert, welches zu 4-ANPP reduziert wird. Die herkömmliche Propionylierung ergibt das Endprodukt in einer Gesamtausbeute von 50 bis 80 %.[84] In verschiedenen Ländern machten klandestin Fentanyl produzierende Labore in den frühen 2000er Jahren Gebrauch vom Siegfried-Verfahren.[85] Eine ausbeutenoptimierte Variante, die einen reduktiven Aminierungsschritt enthält, stellten Valdez et al. im Jahr 2014 vor.[86]
Gupta-Methode
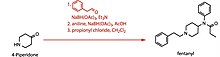
Ein Eintopfverfahren aus dem Jahr 2005 folgt einer reduktiven Tandem-Aminierung, die Natriumtriacetoxyborhydrid (NTAB) als Reagenz verwendet. Dabei reagiert Phenylacetaldehyd mit 4-Piperidinon zu NPP, und zwar chemoselektiv, da der Aldehyd die reaktivere Carbonylkomponente ist. Das Keton reagiert anschließend mit Anilin in situ zum 4-ANPP. Die abschließende N-Propionylierung erfordert ebenfalls keine Isolation des Ansatzes, da das überschüssige NTAB als Abfangreagenz genügt.[87] Ausbeuten bis zu 81 %[88] und leichte Durchführbarkeit machen dieses Verfahren für eine ökonomische Massenproduktion attraktiv. Entsprechend ist das Gupta-Verfahren in der illegalen Fentanyl-Produktion der Gegenwart vorherrschend, wie sich im Jahr 2021 auf Grundlage einer Profiling-Analyse herausstellte, welche 318 in den Vereinigten Staaten beschlagnahmte fentanylhaltige Drogenpräparate untersuchte. Der durchschnittliche Fentanylanteil der Proben betrug 13,6 %, die Spanne reichte von 0,2 % bis 36,4 %. Ein hoher Anteil herkömmlicher Streckstoffe wurde dabei identifiziert.[89]
Analytik
Zur sicheren qualitativen und quantitativen Bestimmung von Fentanyl in Blut-/Blutplasmaproben und Urin wird nach angemessener Probenvorbereitung die Kopplung der Gaschromatographie oder HPLC mit der Massenspektrometrie eingesetzt.[90][91][92][93] Zur Dopingkontrolle werden diese Methoden ebenfalls angewandt.[94] Auch Immunassays[95][96] und elektrochemische Analysen (Voltammetrie, Potentiometrie und Elektrochemilumineszenz)[97] finden Verwendung. Typische Blut- oder Plasmakonzentrationen von Fentanyl im Menschen sind 0,3–3,0 μg/L bei medizinischem Gebrauch, 1–10 μg/L in Drogenkonsumenten und 3–300 μg/L bei akuter Überdosierung.[98] Ein qualitativer Schnelltest kann mit dem Marquis-Reagenz durchgeführt werden.
Auch für forensische Untersuchungen kommen diese Verfahren zum Einsatz.[99][100] In der Forensik gibt es nur eine geringe Korrelation zwischen der ante-mortem-Blutkonzentration von Fentanyl und der post-mortem-Blutkonzentration.[101] Daneben erfolgt nach dem Tod eine Umverteilung des Fentanyls.[102]
Rechtslage
Fentanyl ist als Arznei- und Rauschmittel unter anderem dem deutschen und Schweizer Betäubungsmittelgesetz sowie dem österreichischen Suchtmittelgesetz unterstellt. In den Niederlanden ist Fentanyl eine Substanz der Liste I des Opium-Gesetzes.[103] In Estland wird Fentanyl seit den frühen 2000ern am längsten zum nichtmedizinischen Gebrauch verwendet, und zwar seit die Taliban den Anbau von Schlafmohn in Afghanistan verboten haben.[104] In Großbritannien zählt Fentanyl als controlled Class A drug nach dem Misuse of Drugs Act 1971.[105]
In den Vereinigten Staaten ist Fentanyl eine Schedule II controlled substance nach dem Controlled Substance Act. Vertreiber von Abstral sind verpflichtet, am FDA-genehmigten Risk-Evaluation-and-Mitigation-Strategy-Programm teilzunehmen (REMS).[106][107] Zur Vermeidung von Missbrauch verlangen in den Vereinigten Staaten einige Versicherer Vorzertifizierung und/oder Mengenbegrenzung für Verschreibungen von Actiq.[108][109][110] In Kanada ist Fentanyl eine Droge der Liste I nach dem Controlled Drugs and Substances Act.[111] Laut einem Bericht in The Guardian von 2018 haben viele große Drogenhändler im Dark Web selbsttätig den Handel mit Fentanyl eingestellt.[112]
Veterinärmedizin
Fentanyl wird zur Sedierung und Schmerztherapie in Kleintieren verwendet. Im Vergleich zu anderen Opioiden erzeugt es in Kleintieren weniger Erbrechen, eine tiefere Sedierung und weniger kardiovaskuläre Effekte.[113][114][115] Wie andere Opioide wird Fentanyl in Hunden mit Dysphorie assoziiert.[116]
Zur Behandlung chronischer Schmerzustände stehen aus der Humanmedizin transdermale Verabreichungssysteme zur Verfügung, die auch bei Kleintieren eingesetzt werden können[117] (off label). Die 2012 in der EU und den USA neu im Markt eingeführte transdermale Lösung für die einmalige Anwendung gegen postoperative Schmerzen bei Hunden (Recuvyra) vermarktet der Hersteller nicht mehr.[118][119]
Drogenmissbrauch


Spätestens seit 2006 nimmt der Missbrauch von Fentanyl in den Vereinigten Staaten zu. In einem Bericht sprach das CDC von 1000 Toten zwischen 2005 und 2007; die meisten Fälle wurden in Chicago, Philadelphia und Detroit registriert.[122] Ab 2013 waren Fentanyl und seine Analoga vermehrt in den Vereinigten Staaten auf dem Schwarzmarkt erhältlich.[76] Die daraus folgende Zunahme an Überdosis-Toten durch Fentanyl wird in den Vereinigten Staaten als dritte Welle der Drogentoten-Epidemie bezeichnet.[123] Im Jahr 2014 waren es 4200 Tote.[124] Vorläufige Daten zeigen, dass Fentanyl für einen großen Teil der geschätzt 59.000 bis 65.000 Drogentoten des Jahres 2016 in den Vereinigten Staaten ursächlich war. Im Bezirk Montgomery County wurde im Januar und Februar 2017 bei 99 von 100 Drogentoten Fentanyl oder ein Analogon nachgewiesen.[125] Laut New York Times starben allein auf Long Island 2016 mindestens 220 Menschen durch den Missbrauch von Fentanyl.[126] Von den über 90.000 Personen, die im Jahr 2020 in den Vereinigten Staaten an einer Überdosis starben, nahm jede zweite Fentanyl.[127] Im Jahr 2021 starben in den USA 70.000 Menschen an Fentanyl. Es ist für Amerikaner in der Altersgruppe zwischen 18 und 45 Jahren die häufigste Todesursache.[128] Die Drug Enforcement Administration (DEA) beschlagnahmte 2022 mehr als 4500 kg Fentanyl und über 50 Millionen Fentanyltabletten – mehr als doppelt soviel wie 2021 und genug, um die gesamte Bevölkerung der Vereinigten Staaten zu töten.[129]
Ein Grund für die hohen Todesraten bei Fentanylanwendungen ist die geringe therapeutische Breite.[130] Während eine therapeutische Dosis injizierten Fentanyls über 0,02 mg/kg Körpergewicht nur bei Anwendung der Herz-Lungen-Maschine möglich ist, liegt die letale injizierte Dosis für (Rhesus-)Affen bereits bei 0,03 mg/kg Körpergewicht.[131] Fentanyl kann so schon in einer Menge ab 2 mg für einen erwachsenen, normalgewichtigen Menschen tödlich sein.[132][133]
Eine besondere Gefahr geht auch von Fentanyl in Pulverform aus, so wie es als Ausgangsstoff zwecks Verarbeitung zu Fertigarzneimitteln erworben, aber auch auf dem Schwarzmarkt gehandelt wird, um dann z. B. als Injektion oder transnasal (über die Nasenöffnung) eingenommen zu werden. Es sind Zwischenfälle bekannt, in denen unbeabsichtigt das Pulver in der Luft verwirbelt wurde – beispielsweise beim Fallenlassen eines Behälters mit dem Stoff. So kann ungewollt Fentanyl-Aerosol in Nasen- und/oder Mundschleimhaut gelangen. Eine ungewollte Aufnahme über die Haut ist ebenso möglich, hängt jedoch sehr von der Kontaminationsdichte und den Expositionsbedingungen ab. Die chemisch-physikalische Form des Fentanyls (Base oder Salz, Pulver oder Lösung) und die Durchfeuchtung der Haut (etwa durch Schwitzen) beeinflussen die Penetrationsrate. Einer Studie zufolge sind pharmakologische bzw. toxische Wirkungen nur bei sehr hoher Exposition und verschwitzter Haut zu erwarten.[134][135][136]
Fentanyl wird oft mit verschiedenen Zuckern (wie Lactose) oder Mannitol verschnitten.[137] Fentanyl wird auch zum Strecken zahlreicher auf dem Schwarzmarkt erhältlicher Drogenzubereitungen eingesetzt; wie u. a. Heroin, Kokain, Amphetaminen oder ferner auch gepresster Tabletten (wie den berüchtigten „M30“-Fälschungen).[138][139][140] Durch zu hohe Dosierung oder falsche Verteilung des Fentanyls kommt es so regelmäßig zu unwillkürlicher Überdosierung auf Seiten der Konsumenten, was nicht selten zu lebensgefährlichen Atemdepressionen und zum Tode führt, was die Gesamtzahl Drogentoter weltweit nach oben treibt.[141] Fentanyl, das so verwendet oder direkt auf dem Schwarzmarkt verkauft wird, stammt teils aus legaler pharmazeutischer und teils aus illegaler Produktion.[142] Die Verwendung von Fentanyl als Strecksubstanz ist besonders populär, da es – in bereits sehr geringer Dosierung eingesetzt – eine deutliche psychotrope Wirkung erreicht, wodurch die starke Streckung oft viel weniger augenscheinlich ist als die Beimengung von nicht psychotropen Substanzen, wie z. B. Lactose, Glukose, oder Ascorbinsäure. In einigen US-Bundesstaaten ist die Ausrüstung von Rettungs- und Polizeikräften mit lebensrettender Naloxonzubereitung (z. B. zur nasalen Applikation – wie Narcan) Standard.
Überdosierungen werden durch Injektion mit Naloxon behandelt. Zur langfristigen Behandlung der Fentanylabhängigkeit werden experimentelle Impfstoffe untersucht, die Antikörper gegen Fentanyl hervorrufen.[32] Dadurch wird Fentanyl durch die Antikörper gebunden aus dem Blutkreislauf entfernt.[32]
Kampfstoff
Neben ihrem Einsatz in der Medizin wurden Fentanyl-Derivate auch auf ihre Verwendbarkeit als chemische Kampfstoffe hin untersucht.[143][144] Es wurden Vermutungen darüber angestellt, ob ein besonders potentes, in der Humanmedizin nicht zugelassenes Fentanyl-Derivat, das Carfentanyl, in Aerosol-Form bei der Geiselbefreiung im Moskauer Dubrowka-Theater im Oktober 2002 zum Einsatz kam und dabei für 127 Todesfälle durch Atemstillstand mitursächlich war.[145]
Ein Derivat des Fentanyls wurde von einem israelischen Mossad-Kommando 1997 beim Mordanschlag auf Chalid Maschal in Jordanien eingesetzt.[146] Es wirkte viel stärker als Fentanyl, wurde wie dieses durch die Haut aufgenommen (es wurde am Kopf aufgesprüht) und sollte in wenigen Tagen mit dem Anschein eines natürlichen Todes töten. Die Agenten wurden unmittelbar verhaftet und Israel gab auf diplomatischen Druck daraufhin den Jordaniern die Art des Wirkstoffs bekannt und das wirksame Gegenmittel (Naloxon) mit Anweisungen über die Behandlung.[147]
Hinrichtungsmittel
Fentanyl wurde am 14. August 2018 erstmals als Bestandteil einer Wirkstoffmischung zur Hinrichtung des Doppelmörders Carey Dean Moore im Staatsgefängnis von Nebraska verwendet.[148][149] Der Grund für den Einsatz bei letalen Injektionen in den USA ist die schwieriger werdende Beschaffung der zuvor verwendeten Giftstoffe (u. a. Thiopental) aufgrund eines Liefer- bzw. Produktionsstopps seitens der Hersteller. Auch der US-Bundesstaat Nevada plante den Einsatz von Fentanyl für Hinrichtungen.[150] Nachdem der Hersteller gegen die seiner Meinung nach illegale Anwendung seines Präparats im Juli 2018 geklagt hatte, wurde die Hinrichtung von Scott Dozier ausgesetzt.[151]
Handelsnamen
- Parenteral (intravenös, intramuskulär): Fentanyl B. Braun (D), Fentanyl Hameln (A), Fentanyl Mepha (CH), Sintenyl (CH), u. a.
- Transdermal (transdermales therapeutisches Pflaster): Durogesic (A), Durogesic SMAT (D), Durogesic Matrix (CH), Generika (Fentoron, Matrifen u. a.)
- Oral-transmukosal:
- Buccaltablette: Effentora (EU), Generika
- Buccalfilm: Breakyl (D)
- Lutsch-/Buccaltablette mit integriertem Applikator (Elan Pharma/Teva): Actiq (D, A, CH)
- Sublingualtablette: Abstral (D)
- Nasal-transmukosal (Nasenspray): PecFent (Archimedes Pharma), Instanyl (Takeda)
- Für Tiere (Hunde): Fentadon (D, A)
Literatur
- Eberhard Klaschik: Schmerztherapie und Symptomkontrolle in der Palliativmedizin. In: Stein Husebø, Eberhard Klaschik (Hrsg.): Palliativmedizin. 5. Auflage. Springer, Heidelberg 2009, ISBN 3-642-01548-4, S. 207–313, hier: S. 233 f., 251 f. und 466 f.
- Sam Quinones: The Least of Us: True Tales of America and Hope in the Time of Fentanyl and Meth. Bloomsbury, New York 2021, ISBN 978-1-63557-435-7.
- Michael A. Überall: Transmukosale Applikation von Fentanyl: sublingual, buccal, nasal – egal? In: MMW – Fortschritte der Medizin. Band 159, S6, 2017, S. 15–22, doi:10.1007/s15006-017-0081-1.
Weblinks
- Fentanyl. In: Erowid. (englisch)
- Fentanyl-Arzneimittel auf der Website der Europäischen Arzneimittelagentur (Europäischer Öffentlicher Beurteilungsbericht, EPAR)
Einzelnachweise
- ↑ INN Recommended List 6, World Health Organisation (WHO), 9. November 1966.
- ↑ a b Europäische Arzneibuch-Kommission (Hrsg.): Europäische Pharmakopöe 5. Ausgabe. Band 5.0–5.7, 2006.
- ↑ David R. Lide (Hrsg.): CRC Handbook of Chemistry and Physics. 95. Auflage. (Internet-Version: 2015), CRC Press / Taylor and Francis, Boca Raton FL, Physical Constants of Organic Compounds, S. 3-272.
- ↑ Royal Pharmaceutical Society (Hrsg.): Clarke’s Analysis of Drugs and Poisons FOURTH EDITION. Pharmaceutical Press, London / Chicago 2011, ISBN 978-0-85369-711-4.
- ↑ Samir D. Roy, Gordon L. Flynn: Solubility and Related Physicochemical Properties of Narcotic Analgesics. In: Pharmaceutical Research. Band 5, Nr. 9, 1988, S. 580–586, doi:10.1023/A:1015994030251.
- ↑ a b Datenblatt Fentanyl citrate salt bei Sigma-Aldrich, abgerufen am 4. November 2021 (PDF).
- ↑ Joseph Knoll, Susanna Fürst, Krisztina Kelemen: The pharmacology of azidomorphine and azidocodeine. In: The Journal of Pharmacy and Pharmacology. Band 25, Nr. 12, 1973, S. 929–939, doi:10.1111/j.2042-7158.1973.tb09982.x, PMID 4150295.
- ↑ R. S. Vartanyan, V. O. Martirosyan, S. A. Vartanyan, A. P. Engoyan, É. V. Vlasenko, L. K. Durgaryan, A. S. Azlivyan, A. V. Val'dman: Stereochemistry and biological activity of the novel narcotic analgesic fenaridine. In: Pharmaceutical Chemistry Journal. Band 23, Nr. 5, 1989, S. 395–401, doi:10.1007/BF00758291.
- ↑ Willem F. M. Van Bever, Carlos J. E. Niemegeers, Paul A. J. Janssen: Synthetic analgesics. Synthesis and pharmacology of the diastereoisomers of N-[3-methyl-1-(2-phenylethyl)-4-piperidyl]-N-phenylpropanamide and N-[3-methyl-1-(1-methyl-2-phenylethyl)-4-piperidyl]-N-phenylpropanamide. In: Journal of Medicinal Chemistry. Band 17, Nr. 10, 1974, S. 1047–1051, doi:10.1021/jm00256a003.
- ↑ WHO Model List of Essential Medicines. (PDF) In: World Health Organization. Oktober 2013, archiviert vom (nicht mehr online verfügbar) am 23. April 2014; abgerufen am 22. April 2014 (englisch).
- ↑ a b c Norbert Roewer, Holger Thiel: Taschenatlas der Anästhesie. ISBN 978-3-13-128784-7, 2010. S. 70ff.
- ↑ U.S. Overdose Deaths In 2021 Increased Half as Much as in 2020 - But Are Still Up 15%. In: cdc.gov. 11. Mai 2022, abgerufen am 24. Januar 2023 (englisch).
- ↑ a b T. H. Stanley: The history and development of the fentanyl series. In: Journal of pain and symptom management. Band 7, Nummer 3 Suppl, April 1992, S. S3–S7, doi:10.1016/0885-3924(92)90047-l, PMID 1517629.
- ↑ a b c T. H. Stanley: The Fentanyl Story. In: The Journal of Pain, Band 15, Nummer 12, Dezember 2014, S. 1215–1226, doi:10.1016/j.jpain.2014.08.010
- ↑ Silvia L. Cruz: Opioids. Springer International Publishing 2022, ISBN 978-3-031-09935-9, doi:10.1007/978-3-031-09936-6. S. 165.
- ↑ J. Black: A personal perspective on Dr. Paul Janssen. In: Journal of medicinal chemistry. Band 48, Nummer 6, März 2005, S. 1687–1688, doi:10.1021/jm040195b, PMID 15771410.
- ↑ DailyMed: FENTANYL CITRATE injection, solution (Hospira, Inc.).
- ↑ M. P. Davis, B. Behm: Reasons to avoid fentanyl. In: Annals of palliative medicine. Band 9, Nummer 2, März 2020, S. 611–624, doi:10.21037/apm.2020.01.12, PMID 32156127.
- ↑ Fentanyl (sublimaze). In: Clinical Pharmacology and Therapeutics. 9. Jahrgang, Nr. 5, September 1968, S. 704–706, doi:10.1002/cpt196895704, PMID 5676808.
- ↑ P. Armenian, K. T. Vo, J. Barr-Walker, K. L. Lynch: Fentanyl, fentanyl analogs and novel synthetic opioids: A comprehensive review. In: Neuropharmacology. Band 134, Pt AMai 2018, S. 121–132, doi:10.1016/j.neuropharm.2017.10.016, PMID 29042317.
- ↑ a b R. S. Vardanyan, V. J. Hruby: Fentanyl-related compounds and derivatives: current status and future prospects for pharmaceutical applications. In: Future Medicinal Chemistry. Band 6, Nummer 4, März 2014, S. 385–412, doi:10.4155/fmc.13.215, PMID 24635521, PMC 4137794 (freier Volltext).
- ↑ P. F. Lipiński, J. Matalińska: Fentanyl Structure as a Scaffold for Opioid/Non-Opioid Multitarget Analgesics. In: International Journal of Molecular Sciences. Band 23, Nummer 5, März 2022, S. , doi:10.3390/ijms23052766, PMID 35269909, PMC 8910985 (freier Volltext).
- ↑ Mandal A: Fentanyl History. In: News-Medical.net. AZoNetwork, 11. April 2010, abgerufen am 27. Januar 2023 (englisch).
- ↑ ACTIQ® (fentanyl citrate) oral transmucosal lozenge (1968 version revised in 2011). U.S. Food and Drug Administration (FDA), Dezember 2011, abgerufen am 26. Dezember 2017.
- ↑ Questions and Answers about Onsolis (fentanyl buccal soluble film). U.S. Food and Drug Administration (FDA), 16. Juli 2009, archiviert vom am 22. Juli 2017; abgerufen am 26. Dezember 2017.
- ↑ Matej Mikulic: Fentanyl consumption by country worldwide 2018–2020 – Statista. In: statista.com. 13. April 2022, abgerufen am 29. Januar 2023 (englisch).
- ↑ 2022 Aggregate Production Quota History for Selected Substances.
- ↑ Y. Han, W. Yan, Y. Zheng, M. Z. Khan, K. Yuan, L. Lu: The rising crisis of illicit fentanyl use, overdose, and potential therapeutic strategies. In: Translational psychiatry. Band 9, Nummer 1, November 2019, S. 282, doi:10.1038/s41398-019-0625-0, PMID 31712552, PMC 6848196 (freier Volltext).
- ↑ a b Silvia L. Cruz: Opioids. Springer International Publishing 2022, ISBN 978-3-031-09935-9, doi:10.1007/978-3-031-09936-6. S. 53, 87.
- ↑ H. E. Schueler: Emerging Synthetic Fentanyl Analogs. In: Academic forensic pathology. Band 7, Nummer 1, März 2017, S. 36–40, doi:10.23907/2017.004, PMID 31239954, PMC 6474477 (freier Volltext).
- ↑ Holger Thiel, Norbert Roewer: Anästhesiologische Pharmakotherapie. Allgemeine und spezielle Pharmakologie in Anästhesie, Intensivmedizin, Notfallmedizin und Schmerztherapie. Georg Thieme, Stuttgart / New York 2004, ISBN 3-13-138261-9, S. 173–176.
- ↑ a b c d Y. Han, L. Cao, K. Yuan, J. Shi, W. Yan, L. Lu: Unique Pharmacology, Brain Dysfunction, and Therapeutic Advancements for Fentanyl Misuse and Abuse. In: Neuroscience bulletin. Band 38, Nummer 11, November 2022, S. 1365–1382, doi:10.1007/s12264-022-00872-3, PMID 35570233, PMC 9107910 (freier Volltext).
- ↑ a b S. Mohsin, Z. Ahmad Ganaie, H. Kundi, M. B. Ahmed, B. Riaz, N. Khurshid Ahmed, V. Anirudh Chunchu, A. Haq: Comparison of Fentanyl and Dexmedetomidine in Preventing an Increase in Heart Rate During Intubation Among Patients Undergoing General Anesthesia: A Meta-Analysis. In: Cureus. Band 14, Nummer 6, Juni 2022, S. e26194, doi:10.7759/cureus.26194, PMID 35891845, PMC 9306395 (freier Volltext).
- ↑ P. J. Wiffen, B. Wee, S. Derry, R. F. Bell, R. A. Moore: Opioids for cancer pain - an overview of Cochrane reviews. In: The Cochrane database of systematic reviews. Band 7, Nummer 7, Juli 2017, S. CD012592, doi:10.1002/14651858.CD012592.pub2, PMID 28683172, PMC 6483487 (freier Volltext).
- ↑ G. E. Plante, T. B. VanItallie: Opioids for cancer pain: the challenge of optimizing treatment. In: Metabolism: clinical and experimental. Band 59 Suppl 1, Oktober 2010, S. S47–S52, doi:10.1016/j.metabol.2010.07.010, PMID 20837194.
- ↑ Shachtman N: Airborne EMTs Shave Seconds to Save Lives in Afghanistan. In: Wired. 10. September 2009 (wired.com ( des vom 6. Juli 2010 im Internet Archive) [abgerufen am 1. Juli 2010]).
- ↑ S. J. Friedrichsdorf: From Tramadol to Methadone: Opioids in the Treatment of Pain and Dyspnea in Pediatric Palliative Care. In: The Clinical journal of pain. Band 35, Nummer 6, Juni 2019, S. 501–508, doi:10.1097/AJP.0000000000000704, PMID 30985399.
- ↑ E. C. Moisés, L. de Barros Duarte, R. de Carvalho Cavalli, V. L. Lanchote, G. Duarte, S. P. da Cunha: Pharmacokinetics and transplacental distribution of fentanyl in epidural anesthesia for normal pregnant women. In: European Journal of Clinical Pharmacology. Band 61, Nummer 7, August 2005, S. 517–522, doi:10.1007/s00228-005-0967-9, PMID 16021436.
- ↑ a b J. A. Nanji, B. Carvalho: Pain management during labor and vaginal birth. In: Best practice & research. Clinical obstetrics & gynaecology. Band 67, August 2020, S. 100–112, doi:10.1016/j.bpobgyn.2020.03.002, PMID 32265134.
- ↑ N. M. Fonseca, G. M. Guimarães, J. P. Pontes, L. M. Azi, R. de Ávila Oliveira: Safety and effectiveness of adding fentanyl or sufentanil to spinal anesthesia: systematic review and meta-analysis of randomized controlled trials. In: Brazilian journal of anesthesiology. Dezember 2021, doi:10.1016/j.bjane.2021.10.010, PMID 34954261.
- ↑ a b c B. A. Baldo, M. A. Rose: The anaesthetist, opioid analgesic drugs, and serotonin toxicity: a mechanistic and clinical review. In: British journal of anaesthesia. Band 124, Nummer 1, Januar 2020, S. 44–62, doi:10.1016/j.bja.2019.08.010, PMID 31653394.
- ↑ S. A. Schug, S. Ting: Fentanyl Formulations in the Management of Pain: An Update. In: Drugs. Band 77, Nummer 7, Mai 2017, S. 747–763, doi:10.1007/s40265-017-0727-z, PMID 28337672.
- ↑ Zusammenfassung der Merkmale des Arzneimittels Instanyl®. (PDF; 1002 kB) Stand: 20. Juli 2009, Website der Europäischen Arzneimittelagentur EMEA; abgerufen am 1. Oktober 2009.
- ↑ a b c d e f Hemmings HC, Egan TD: Pharmacology and Physiology for Anesthesia: Foundations and clinical application. 2. Auflage. Philadelphia, PA 2018, ISBN 978-0-323-56886-9.
- ↑ a b Fentanyl, Fentanyl Citrate, Fentanyl Hydrochloride. The American Society of Health-System Pharmacists, abgerufen am 8. Dezember 2017.
- ↑ a b Fentanyl side effects in detail. In: Drugs.com. Abgerufen am 16. Juni 2018.
- ↑ S. Mayes, M. Ferrone: Fentanyl HCl patient-controlled iontophoretic transdermal system for the management of acute postoperative pain. In: The Annals of pharmacotherapy. Band 40, Nummer 12, Dezember 2006, S. 2178–2186, doi:10.1345/aph.1H135, PMID 17164395.
- ↑ David W Chambers, Christopher L.-H. Huang, Gareth B. Matthews: Anaesthesia and the lung. In: Cambridge University Press eBooks. 2015, S. 107–110. doi:10.1017/CBO9781139226394.027.
- ↑ R. Torralva, A. Janowsky: Noradrenergic Mechanisms in Fentanyl-Mediated Rapid Death Explain Failure of Naloxone in the Opioid Crisis. In: The Journal of pharmacology and experimental therapeutics. Band 371, Nummer 2, November 2019, S. 453–475, doi:10.1124/jpet.119.258566, PMID 31492824, PMC 6863461 (freier Volltext).
- ↑ Rote-Hand-Brief. (PDF) BfArM, 12. Juni 2014; abgerufen am 20. Juni 2014
- ↑ Fentanyl patch can be deadly to children. U.S. Food and Drug Administration (FDA), 19. April 2012, abgerufen am 30. Juli 2013.
- ↑ Accidental Exposures to Fentanyl Patches Continue to Be Deadly to Children. U.S. Food and Drug Administration (FDA), 21. Juli 2021, abgerufen am 29. April 2023 (englisch).
- ↑ FDA Approves First Over-the-Counter Naloxone Nasal Spray, FDA, 29. März 2023.
- ↑ J. Christensen: FDA advisers vote in favor of making opioid overdose antidote available over the counter, CNN, 15. Februar 2023.
- ↑ Fentanyl (transdermal patches, solution for injection - nationally authorised product only) - CMDh Scientific conclusions and grounds for variation, amendments to the Product Information and timetable for the implementation - PSUSA/00001370/202204 (PDF/168.84 KB), www.ema.europa.eu, 23. Januar 2023.
- ↑ P.A. Herman, D.S. Brenner, S. Dandorf, S. Kemp, B. Kroll, J. Trebach, Y.H. Hsieh, A.I. Stolbach: Media Reports of Unintentional Opioid Exposure of Public Safety First Responders in North America. In: Journal of Medical Toxicology. 16. Jahrgang, Nr. 2, April 2020, S. 112–115, doi:10.1007/s13181-020-00762-y, PMID 32096007, PMC 7099103 (freier Volltext) – (englisch).
- ↑ Fentanyl Transdermal System (marketed as Duragesic) Information. In: FDA ALERT 7/15/2005; Update 12/21/2007. 30. September 2009, abgerufen am 26. August 2010 (englisch).
- ↑ Reported Patient Deaths Increased by 14 % in 2009. (68 kB; PDF) In: QuarterWatch: 2009 Quarter 4. Institute for Safe Medication Practices, 16. Juni 2010, S. 2, archiviert vom (nicht mehr online verfügbar) am 4. Dezember 2010; abgerufen am 26. August 2010 (englisch, US 501c (3) nonprofit organization): „In 2009 fentanyl products accounted for 397 reported patient deaths, ranked 4th among all drugs“.
- ↑ Deutsches Ärzteblatt. Jg. 109, Heft 14, 6. April 2012 (PDF; 259 kB) abgerufen von Website der Arzneimittelkommission der deutschen Ärzteschaft (AkdÄ).
- ↑ B. R. Overholser, D. R. Foster: Opioid pharmacokinetic drug-drug interactions. In: The American journal of managed care. Band 17 Suppl 11, September 2011, S. S276–S287, PMID 21999760.
- ↑ B. Bormann, J. Boldt, G. Sturm, D. Kling, B. Weidler, E. Lohmann, G. Hempelmann: Calcium antagonists in anesthesia. Additive analgesia using nimodipine in heart surgery. In: Anaesthesist. 34, 1985, S. 429. PMID 4083464.
- ↑ J. Boldt, B. von Bormann, D. Kling, W. Russ, K. Ratthey, G. Hempelmann: Low-dose fentanyl analgesia modified by calcium channel blockers in cardiac surgery. In: Eur. J. Anesth. 4(6), 1987, S. 387. PMID 3328680
- ↑ Rote-Hand-Briefe zu Fentanyl®-Janssen und Durogesic SMAT (12, 25, 50, 75, 100 µg/h), transdermales Pflaster (Wirkstoff: Fentanyl): Neuer Warnhinweis. Mitteilung der Bundesoberbehörde BfArM, 11. März 2013; abgerufen am 22. September 2015.
- ↑ Raynor K, Kong H, Chen Y, Yasuda K, Yu L, Bell GI, Reisine T: Pharmacological characterization of the cloned kappa-, delta-, and mu-opioid receptors. In: Molecular Pharmacology. 45. Jahrgang, Nr. 2, Februar 1994, S. 330–334, PMID 8114680 (englisch).
- ↑ a b c d E. Kelly, K. Sutcliffe, D. Cavallo, N. Ramos-Gonzalez, N. Alhosan, G. Henderson: The anomalous pharmacology of fentanyl. In: British journal of pharmacology. Mai 2021, doi:10.1111/bph.15573, PMID 34030211.
- ↑ a b J. Lötsch, C. Walter, M. J. Parnham, B. G. Oertel, G. Geisslinger: Pharmacokinetics of non-intravenous formulations of fentanyl. In: Clinical Pharmacokinetics. Band 52, Nummer 1, Januar 2013, S. 23–36, doi:10.1007/s40262-012-0016-7, PMID 23100195.
- ↑ D. Häske und andere: Analgesie bei Traumapatienten in der Notfallmedizin. In: Der Anaesthesist, Band 69, Nr. 2, Februar 2020, S. 137–148, hier: S. 141 (Wirkbeginn bei 0,6–2,5 µg/kgKG und intravenöser Gabe: 1–2 Minuten).
- ↑ James M. Ritter, Rod Flower, Graeme Henderson, Yoon Kong Loke, David MacEwan, and Humphrey P. Rang: Rang & Dale's Pharmacology. 9. Auflage 2020. Elsevier. ISBN 978-0-7020-7448-6. S. 556.
- ↑ a b G. Geisslinger et al.: Mutschler Arzneimittelwirkungen. 11. Auflage. WVG, Stuttgart 2019, S. 304.
- ↑ M. Schäfer, C. Zöllner: Opioide in der Anästhesiologie. In: Rossaint et al. (Hrsg.): Die Anästhesiologie. Springer Reference Medizin. Springer, Berlin, Heidelberg. 2016. S. 1–24.
- ↑ Fachinformation Fentanyl-Hexal 0,1 mg / 0,5 mg Injektionslösung, Stand März 2022. Hexal AG.
- ↑ Fachinformation Durogesic SMAT Transdermales Pflaster. Stand März 2022. Janssen-Cilag GmbH.
- ↑ a b D.K. Gupta, T.C. Krejcie, M.J. Avram: Pharmacokinetics of opioids. In: Anesthetic Pharmacology (Hrsg.: A.S. Evers, M. Maze, E.D. Kharasch) Cambridge University Press, 2011. S. 509–530. doi:10.1017/cbo9780511781933.033
- ↑ Eberhard Klaschik: Schmerztherapie und Symptomkontrolle in der Palliativmedizin. 2009, S. 233 f.
- ↑ D. Häske und andere: Analgesie bei Traumapatienten in der Notfallmedizin. In: Der Anaesthesist, Band 69, Nr. 2, Februar 2020, S. 137–148, hier: S. 141.
- ↑ a b S. D. Comer, C. M. Cahill: Fentanyl: Receptor pharmacology, abuse potential, and implications for treatment. In: Neuroscience and biobehavioral reviews. Band 106, November 2019, S. 49–57, doi:10.1016/j.neubiorev.2018.12.005, PMID 30528374, PMC 7233332 (freier Volltext).
- ↑ Tom Peck and Benjamin Harris: Pharmacology for Anaesthesia and Intensive Care. 5. Auflage 2021, Oxford University Press. ISBN 978-1-108-71096-1. doi:10.1017/9781108591317. S. 136.
- ↑ Wilde M, Pichini S, Pacifici R, Tagliabracci A, Busardò FP, Auwärter V, Solimini R: Metabolic Pathways and Potencies of New Fentanyl Analogs. In: Front Pharmacol. 10. Jahrgang, 2019, S. 238, doi:10.3389/fphar.2019.00238, PMID 31024296, PMC 6461066 (freier Volltext).
- ↑ V. C. Ziesenitz, J. D. Vaughns, G. Koch, G. Mikus, J. N. van den Anker: Correction to: Pharmacokinetics of Fentanyl and Its Derivatives in Children: A Comprehensive Review. In: Clinical Pharmacokinetics. Band 57, Nummer 3, März 2018, S. 393–417, doi:10.1007/s40262-017-0609-2, PMID 29178007.
- ↑ R. Tao, M. Karnik, Z. Ma, S. B. Auerbach: Effect of fentanyl on 5-HT efflux involves both opioid and 5-HT1A receptors. In: British journal of pharmacology. Band 139, Nummer 8, August 2003, S. 1498–1504, doi:10.1038/sj.bjp.0705378, PMID 12922937, PMC 1573976 (freier Volltext).
- ↑ Tschirhart JN, Zhang S: Fentanyl-Induced Block of hERG Channels Is Exacerbated by Hypoxia, Hypokalemia, Alkalosis, and the Presence of hERG1b. In: Mol Pharmacol. 98. Jahrgang, Nr. 4, 2020, S. 508–517, doi:10.1124/mol.119.119271, PMID 32321735.
- ↑ Y. Zhuang, Y. Wang, B. He, et al.: Molecular recognition of morphine and fentanyl by the human μ-opioid receptor. In: Cell. Band 185, Nummer 23, November 2022, S. 4361–4375.e19, doi:10.1016/j.cell.2022.09.041, PMID 36368306.
- ↑ Fentanyl Synthesis. In: GPTA India. 18. Juni 2020.
- ↑ Siegfried, Synthesis of Fentanyl, Erowid-Archiv.
- ↑ Designation of Benzylfentanyl and 4-Anilinopiperidine, Precursor Chemicals Used in the Illicit Manufacture of Fentanyl, as List I Chemicals. In: federalregister.gov. DEA, 15. April 2020, abgerufen am 28. Januar 2023.
- ↑ Valdez CA, Leif RN, Mayer BP (2014): An Efficient, Optimized Synthesis of Fentanyl and Related Analogs. Plos One.
- ↑ Gupta PK, Ganesan K, Pande A, Malhotra RC (2005): A convenient one pot synthesis of fentanyl. J. Chem. Res., S. 452,
- ↑ Asadi Z, et al. (2017): A structural study of fentanyl by DFT calculations, NMR and IR spectroscopy. J. Mol. Struct., S. 552.
- ↑ Fentanyl Profiling Program Report. In: Special Testing and Research Laboratory. Drug Enforcement Administration, S. 1–2, abgerufen am 25. Januar 2023.
- ↑ B. A. Goldberger, C. W. Chronister, M. L. Merves: Quantitation of fentanyl in blood and urine using gas chromatography-mass spectrometry (GC-MS). In: Methods Mol Biol., 603, 2010, S. 245–252. PMID 20077075.
- ↑ S. Q. Cheng, D. S. Ouyang, Y. J. Tang, K. Wu, J. Xiao: A rapid, simple and sensitive method for the determination and bioequivalence study of transdermal fentanyl in human plasma using liquid chromatography-electrospray ionization tandem mass spectrometry. In: Int J Clin Pharmacol Ther., 54(2), Feb 2016, S. 144–156. PMID 26754304.
- ↑ R. L. Shaner, P. Kaplan, E. I. Hamelin, W. A. Bragg, R. C. Johnson: Comparison of two automated solid phase extractions for the detection of ten fentanyl analogs and metabolites in human urine using liquid chromatography tandem mass spectrometry. In: J Chromatogr B Analyt Technol Biomed Life Sci., 962, 1. Juli 2014, S. 52–58. PMID 24893271.
- ↑ C. A. Valdez: Gas Chromatography-Mass Spectrometry Analysis of Synthetic Opioids Belonging to the Fentanyl Class: A Review. In: Critical reviews in analytical chemistry. Band 52, Nummer 8, 2022, S. 1938–1968, doi:10.1080/10408347.2021.1927668, PMID 34053394.
- ↑ M. Thevis, H. Geyer, D. Bahr, W. Schänzer: Identification of fentanyl, alfentanil, sufentanil, remifentanil and their major metabolites in human urine by liquid chromatography/tandem mass spectrometry for doping control purposes. In: Eur J Mass Spectrom., (Chichester). 11(4), 2005, S. 419–427. PMID 16204809.
- ↑ S. M. Thomasy, K. R. Mama, S. D. Stanley: Comparison of liquid chromatography-mass spectrometry and radioimmunoassay for measurement of fentanyl and determination of pharmacokinetics in equine plasma. In: J Anal Toxicol., 32(9), Nov-Dez 2008, S. 754–759. PMID 19021930.
- ↑ T. Tobin, H. H. Tai, C. L. Tai, P. K. Houtz, M. R. Dai, W. E. Woods, J. M. Yang, T. J. Weckman, S. L. Chang, J. W. Blake u. a.: Immunoassay detection of drugs in racing horses. IV. Detection of fentanyl and its congeners in equine blood and urine by a one step ELISA assay. In: Res Commun Chem Pathol Pharmacol., 60(1), April 1988, S. 97–115. PMID 2967991.
- ↑ M. K. Choińska, I. Šestáková, V. Hrdlička, J. Skopalová, J. Langmaier, V. Maier, T. Navrátil: Electroanalysis of Fentanyl and Its New Analogs: A Review. In: Biosensors. Band 12, Nummer 1, Januar 2022, S. , doi:10.3390/bios12010026, PMID 35049654, PMC 8774265 (freier Volltext).
- ↑ Baselt, R. (2017) Disposition of Toxic Drugs and Chemicals in Man, 11th edition, Biomedical Publications, Foster City, CA, pp. 883–886.
- ↑ J. Poklis, A. Poklis, C. Wolf, M. Mainland, L. Hair, K. Devers, L. Chrostowski, E. Arbefeville, M. Merves, J. Pearson: Postmortem tissue distribution of acetyl fentanyl, fentanyl and their respective nor-metabolites analyzed by ultrahigh performance liquid chromatography with tandem mass spectrometry. In: Forensic Sci Int., 257, Dez 2015, S. 435–441. PMID 26583960
- ↑ R. Verplaetse, J. Tytgat: Development and validation of a sensitive ultra performance liquid chromatography tandem mass spectrometry method for the analysis of fentanyl and its major metabolite norfentanyl in urine and whole blood in forensic context. In: J Chromatogr B Analyt Technol Biomed Life Sci., 878(22), 15. Juli 2010, S. 1987–1996. PMID 20542478
- ↑ R. B. Palmer: Fentanyl in postmortem forensic toxicology. In: Clinical toxicology. Band 48, Nummer 8, Oktober 2010, S. 771–784, doi:10.3109/15563650.2010.525514, PMID 20969499.
- ↑ Paul I. Dargan, David M. Wood: Novel Psychoactive Substances: Classification, Pharmacology and Toxicology. 2. Auflage, Academic Press, 2021. ISBN 978-0-12-819030-2. S. 450.
- ↑ Opiumwet. (deutsch: Opium Act of the Ministry of the Interior and Kingdom Relations). In: Ministerie van Binnenlandse Zaken en Koninkrijksrelaties. Abgerufen am 19. Januar 2023 (niederländisch).
- ↑ Naylor A: What we can learn from a tiny Baltic country's two-decade Fentanyl crisis. In: Vice. 6. Januar 2020.
- ↑ Misuse of Drugs Act 1971. Abgerufen am 22. März 2017.
- ↑ RelayHealth's pharmacy connectivity network and reach, aligned with McKesson Specialty Care Solutions' REMS expertise, expands cancer patients' access to pain therapy. 20. Januar 2011, archiviert vom am 29. Januar 2016; abgerufen am 5. November 2015.
- ↑ Shelley S: With a few stumbles, REMS begins to hit its atride. In: Pharmaceutical Commerce. 22. April 2011, archiviert vom am 29. Januar 2016; abgerufen am 5. November 2015.
- ↑ Procedures, programs and drugs that require precertification: Participating provider precertification list. Aetna Inc., archiviert vom am 9. Juli 2021; abgerufen am 4. Juli 2021.
- ↑ Notice regarding precertification requirement. BlueCross BlueShield of Arizona, 5. November 2007, archiviert vom am 28. August 2008.
- ↑ Medications requiring precertification. Oxford Health Plans, archiviert vom am 15. Oktober 2006.
- ↑ Canada's Controlled Drugs and Substances Act. In: laws.justice.gc.ca. Abgerufen am 8. September 2018.
- ↑ Townsend M: Dark web dealers voluntarily ban deadly fentanyl. The Guardian, 1. Dezember 2018, abgerufen am 3. Dezember 2018.
- ↑ Kukanich B, Clark TP: The history and pharmacology of fentanyl: relevance to a novel, long-acting transdermal fentanyl solution newly approved for use in dogs. In: Journal of Veterinary Pharmacology and Therapeutics. 35. Jahrgang, Suppl 2, August 2012, S. 3–19, doi:10.1111/j.1365-2885.2012.01416.x, PMID 22731771.
- ↑ Gutierrez-Blanco E, Victoria-Mora JM, Ibancovichi-Camarillo JA, Sauri-Arceo CH, Bolio-González ME, Acevedo-Arcique CM, Marin-Cano G, Steagall PV: Postoperative analgesic effects of either a constant rate infusion of fentanyl, lidocaine, ketamine, dexmedetomidine, or the combination lidocaine-ketamine-dexmedetomidine after ovariohysterectomy in dogs. In: Veterinary Anaesthesia and Analgesia. 42. Jahrgang, Nr. 3, Mai 2015, S. 309–318, doi:10.1111/vaa.12215, PMID 25039918.
- ↑ Pettifer GR, Dyson DH: Comparison of medetomidine and fentanyl-droperidol in dogs: sedation, analgesia, arterial blood gases and lactate levels. In: Canadian Journal of Veterinary Research = Revue Canadienne de Recherche Veterinaire. 57. Jahrgang, Nr. 2, April 1993, S. 99–105, PMID 8490814, PMC 1263601 (freier Volltext).
- ↑ Becker WM, Mama KR, Rao S, Palmer RH, Egger EL: Prevalence of dysphoria after fentanyl in dogs undergoing stifle surgery. In: Veterinary Surgery. 42. Jahrgang, Nr. 3, April 2013, S. 302–307, doi:10.1111/j.1532-950X.2012.01080.x, PMID 23231071.
- ↑ H.-H. Frey, W. Löscher (Hrsg.): Lehrbuch der Pharmakologie und Toxikologie für die Veterinärmedizin. 3. Auflage, Enke Verlag, 2010. S. 142.
- ↑ Eintrag EU/2/11/127 im Unionsregister, abgerufen am 11. Februar 2023.
- ↑ Federal Register, United States Government, abgerufen am 11. Februar 2023.
- ↑ Fentanyl | DEA.gov. Abgerufen am 2. Februar 2022.
- ↑ Overdose Death Rates. National Institute on Drug Abuse (NIDA), 29. Januar 2021 (englisch).
- ↑ Nonpharmaceutical Fentanyl-Related Deaths — Multiple States, April 2005–March 2007. CDC, MMWR, 25. Juli 2008/57(29), S. 793–796.
- ↑ D. Ciccarone: The rise of illicit fentanyls, stimulants and the fourth wave of the opioid overdose crisis. In: Current opinion in psychiatry. Band 34, Nummer 4, Juli 2021, S. 344–350, doi:10.1097/YCO.0000000000000717, PMID 33965972, PMC 8154745 (freier Volltext).
- ↑ Tom Porter: What is Fentanyl, the Drug Linked to Thousands of Deaths in North America? In: Newsweek.com. 28. April 2017, abgerufen am 11. August 2017.
- ↑ Josh Katz: Drug Deaths in America Are Rising Faster Than Ever. In: New York Times. 5. Juni 2017.
- ↑ Kevin Deutsch: Toll of Fentanyl, more potent than heroin, is rising. In: New York Times. 29. Dezember 2016.
- ↑ Der verheerende Siegeszug von Fentanyl
- ↑ Stefanie Bolzen, Neue Drogen für Europa, In: Welt am Sonntag Frühausgabe vom 6. Mai 2023
- ↑ Matza M: Enough fentanyl to kill every single American seized in 2022. BBC News, 21. Dezember 2022, abgerufen am 21. Dezember 2022.
- ↑ Fentanyl: Hochwirksam und hochgefährlich
- ↑ Akorn Inc.: Fentanyl Citrate Injection, USP,. (PDF) Abgerufen am 15. Juli 2020 (englisch).
- ↑ Lethal vs. Medicinal Doses of Fentanyl. In: oxfordtreatment.com. Abgerufen am 25. September 2018.
- ↑ Fentanyl drug profile. European Monitoring Centre for Drugs and Drug Addiction (EMCDDA) vom 8. Januar 2015, abgerufen am 25. September 2018.
- ↑ Warnmeldung von Interpol zu Risiken im Umgang mit Fentanyl, Fentanylderivaten und sonstigen synthetischen Opioiden. In: aekno.de. Ärztekammer Nordrhein, 2. Oktober 2017, abgerufen am 28. März 2022.
- ↑ Schnelltest für Superdroge Fentanyl - Grenze zum Gift im Nanobereich. Abgerufen am 15. August 2020.
- ↑ Lina Thors, Linda Öberg, Emma Forsberg, Elisabeth Wigenstam, Andreas Larsson: Skin penetration and decontamination efficacy following human skin exposure to fentanyl. In: Toxicology in vitro: an international journal published in association with BIBRA. Band 67, September 2020, S. 104914, doi:10.1016/j.tiv.2020.104914, PMID 32540164.
- ↑ J. Pergolizzi, P. Magnusson, J. A. LeQuang, F. Breve: Illicitly Manufactured Fentanyl Entering the United States. In: Cureus. Band 13, Nummer 8, August 2021, S. e17496, doi:10.7759/cureus.17496, PMID 34603876, PMC 8476199 (freier Volltext).
- ↑ Counterfeit Pills. (PDF) Abgerufen am 30. April 2022 (englisch).
- ↑ K. Kuczyńska, P. Grzonkowski, Kacprzak, J. B. Zawilska: Abuse of fentanyl: An emerging problem to face. In: Forensic science international. Band 289, August 2018, S. 207–214, doi:10.1016/j.forsciint.2018.05.042, PMID 29902699.
- ↑ Anna Żubrycka, Andrzej Kwaśnica, Monika Haczkiewicz, Karolina Sipa, Konrad Rudnicki: Illicit drugs street samples and their cutting agents. The result of the GC-MS based profiling define the guidelines for sensors development. In: Talanta. Band 237, 15. Januar 2022, S. 122904, doi:10.1016/j.talanta.2021.122904.
- ↑ How lethal fentanyl 'hot spots’ end up getting cut into street drugs. In: cbc.ca. 17. Oktober 2016, abgerufen am 11. August 2017.
- ↑ Fentanyl crisis: Is China a major source? In: bbc.com. 24. September 2018, abgerufen am 25. September 2018 (englisch).
- ↑ Medical ethics and non-lethal weapons. In: Am J Bioeth., 4(4), 2004, S. W1–W2. PMID 16192174.
- ↑ Fentanyl and its analogues in clinical and forensic toxicology. In: Przegl Lek., 62(6), 2005, S. 581–584. PMID 16225129.
- ↑ Unexpected “gas” casualties in Moscow: a medical toxicology perspective. In: Ann Emerg Med., 41(5), Mai 2003, S. 700–705. PMID 12712038.
- ↑ Paul McGeough, Kill Khalid, Allen, Unwin. 2009, S. 2, 183 f. McGeough spricht von Levofentanyl, das ein nicht auf den Markt gekommenes und auch in pharmazeutischen Datenbanken damals unbekanntes Forschungs-Nebenprodukt der Firma Janssen Pharmaceutica in New Jersey war, manchmal ist auch von Lofentanil die Rede.
- ↑ Die jordanischen Ärzte hatten aber schon Hinweise aus den bei den israelischen Agenten gefundenen Gegenmitteln. Vgl. Mcgeough, S. 183 f.; siehe auch chemistry.stackexchange.com.
- ↑ Judge clears way for America’s first execution using fentanyl. In: The Telegraph. 11. August 2018 (telegraph.co.uk [abgerufen am 11. August 2018]).
- ↑ Nebraska setzt Fentanyl bei Hinrichtung ein. In: orf.at. August 2018, abgerufen am 14. August 2018.
- ↑ Chris Mc Greal: Nevada to become first state to execute inmate with fentanyl. In: theguardian.com. 10. Juli 2018, abgerufen am 25. September 2018 (englisch).
- ↑ Richard A. Oppel Jr.: Nevada Execution Is Blocked After Drugmaker Sues. In: The New York Times. 11. Juli 2018, abgerufen am 25. September 2018 (englisch).