Eugenylacetat
| Strukturformel | |||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
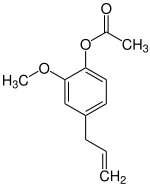
| |||||||||||||||||||
| Allgemeines | |||||||||||||||||||
| Name | Eugenylacetat | ||||||||||||||||||
| Andere Namen | |||||||||||||||||||
| Summenformel | C12H14O3 | ||||||||||||||||||
| Externe Identifikatoren/Datenbanken | |||||||||||||||||||
| |||||||||||||||||||
| Eigenschaften | |||||||||||||||||||
| Molare Masse | 206,24 g·mol−1 | ||||||||||||||||||
| Aggregatzustand |
flüssig | ||||||||||||||||||
| Dichte |
1,079 g·cm−3 (25 °C)[2] | ||||||||||||||||||
| Schmelzpunkt |
23,9 °C[2] | ||||||||||||||||||
| Siedepunkt |
281–286 °C[2] | ||||||||||||||||||
| Löslichkeit |
leicht in Wasser (407 g·l−1 bei 20 °C)[2] | ||||||||||||||||||
| Sicherheitshinweise | |||||||||||||||||||
| |||||||||||||||||||
| Soweit möglich und gebräuchlich, werden SI-Einheiten verwendet. Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen. | |||||||||||||||||||
Eugennylacetat ist ein Carbonsäureester, der sich von Eugenol und Essigsäure ableitet.
Vorkommen
Eugenylacetat kommt im ätherischen Öl der Gewürznelke vor.[3][4] Dieses besteht hauptsächlich aus Eugenol. Unter den Nebenkomponenten ist Eugenylacetat die mengenmäßig wichtigste.[3] Ätherisches Öl aus Anis enthält etwa 3–4 % Eugenylacetat.[5] Es kommt außerdem in den Blättern von Piper betel vor.[6]
Herstellung
Eugenylacetat kann durch Umsetzung von Eugenol und Acetanhydrid unter heterogener saurer Katalyse hergestellt werden.[7]
Eigenschaften
Eugenylacetat kristallisiert im monoklinen Kristallsystem in der Raumgruppe C2/c mit den Parametern a = 11.043, b = 12,095, c = 17.005 und β = 103,055 sowie 8 Formeleinheiten pro Elementarzelle.[8] Der n-Octanol-Wasser-Verteilungskoeffizient liegt bei .[2]
Verwendung
Eugenylacetat ist in der EU unter der FL-Nummer 09.020 als Aromastoff für Lebensmittel allgemein zugelassen.[9]
Sicherheitshinweise
Eugenylacetat hat einen Flammpunkt von 142 °C.[2]
Einzelnachweise
- ↑ Eintrag zu EUGENYL ACETATE in der CosIng-Datenbank der EU-Kommission, abgerufen am 9. Februar 2024.
- ↑ a b c d e f g h Datenblatt Eugenylacetat bei Sigma-Aldrich, abgerufen am 9. Februar 2024 (PDF).
- ↑ a b S. Rovio, K. Hartonen, Y. Holm, R. Hiltunen, M.-L. Riekkola: Extraction of clove using pressurized hot water. In: Flavour and Fragrance Journal. Band 14, Nr. 6, November 1999, S. 399–404, doi:10.1002/(SICI)1099-1026(199911/12)14:6<399::AID-FFJ851>3.0.CO;2-A.
- ↑ Hiroko Kasai, Mika Shirao, Mayumi Ikegami‐Kawai: Analysis of volatile compounds of clove ( syzygium aromaticum ) buds as influenced by growth phase and investigation of antioxidant activity of clove extracts. In: Flavour and Fragrance Journal. Band 31, Nr. 2, März 2016, S. 178–184, doi:10.1002/ffj.3299.
- ↑ R. Omidbaigi, A. Hadjiakhoondi, M. Saharkhiz: Changes in Content and Chemical Composition of Pimpinella anisum Oil at Various Harvest Time. In: Journal of Essential Oil Bearing Plants. Band 6, Nr. 1, Januar 2003, S. 46–50, doi:10.1080/0972-060X.2003.10643328.
- ↑ H. V. Annegowda, P. Y. Tan, M. N. Mordi, S. Ramanathan, M. R. Hamdan, M. H. Sulaiman, S. M. Mansor: TLC–Bioautography-Guided Isolation, HPTLC and GC–MS-Assisted Analysis of Bioactives of Piper betle Leaf Extract Obtained from Various Extraction Techniques: In vitro Evaluation of Phenolic Content, Antioxidant and Antimicrobial Activities. In: Food Analytical Methods. Band 6, Nr. 3, Juni 2013, S. 715–726, doi:10.1007/s12161-012-9470-y.
- ↑ Josiele S. Tischer, Heloysa Possan, José Luiz, Natalia B. Malagutti, Rafael Martello, Alexssandra Valério, Jacir Dalmagro, Débora de Oliveira, J. Vladimir Oliveira: Synthesis of eugenyl acetate through heterogeneous catalysis. In: Journal of Essential Oil Research. Band 31, Nr. 4, 4. Juli 2019, S. 312–318, doi:10.1080/10412905.2019.1566098.
- ↑ Amanda L. dos Santos, Gilberto O. Chierice, Kenneth Alexander, Alan Riga: Crystal Structure Determination for Eugenyl Acetate. In: Journal of Chemical Crystallography. Band 39, Nr. 9, September 2009, S. 655–661, doi:10.1007/s10870-009-9539-7.
- ↑ Food and Feed Information Portal Database | FIP. Abgerufen am 9. Februar 2024.







