„Cyclohexan“ – Versionsunterschied
| [ungesichtete Version] | [ungesichtete Version] |
Keine Bearbeitungszusammenfassung |
Keine Bearbeitungszusammenfassung |
||
| Zeile 24: | Zeile 24: | ||
| [[Aggregatzustand]] || flüssig |
| [[Aggregatzustand]] || flüssig |
||
|- |
|- |
||
| [[Dichte]] || 0, |
| [[Dichte]] || 0,7833 g/cm³ (15 °C) |
||
|- |
|||
| [[thermischer Koeffizient]] || 0,001213 |
|||
|- |
|- |
||
| [[Schmelzpunkt]] || 6,5 [[Grad Celsius|°C]] |
| [[Schmelzpunkt]] || 6,5 [[Grad Celsius|°C]] |
||
Version vom 26. Mai 2006, 18:54 Uhr
| Strukturformel und Kalottemodell | |||
|---|---|---|---|
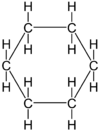 |
 | ||
| Allgemeines | |||
| Name | Cyclohexan | ||
| Andere Namen | Hexahydrobenzol, Hexamethylen, Naphthen | ||
| Summenformel | C6H12 | ||
| CAS-Nummer | 110-82-7 | ||
| Kurzbeschreibung | farblose Flüssigkeit | ||
| Eigenschaften | |||
| Molmasse | 84,16 g/mol | ||
| Aggregatzustand | flüssig | ||
| Dichte | 0,7833 g/cm³ (15 °C) | ||
| thermischer Koeffizient | 0,001213 | ||
| Schmelzpunkt | 6,5 °C | ||
| Siedepunkt | 80,7 °C | ||
| Dampfdruck | 12,7 kPa (? °C) | ||
| Löslichkeit | gut in Alkohol, Ether, unlöslich in Wasser | ||
| Sicherheitshinweise | |||
| Gefahrensymbole | |||
| |||
| R- und S-Sätze |
R: 11-38-50/53-65-67 | ||
| MAK | 300 ml/m³ | ||
| Soweit möglich und gebräuchlich, werden SI-Einheiten verwendet. Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen. | |||
Cyclohexan (auch Hexahydrobenzol, Hexamethylen, Naphthen) ist eine farblose Flüssigkeit. Es ist ein Cycloalkan mit der Summenformel C6H12, das im Erdöl vorkommt und als Lösungsmittel und Grundstoff in der Synthese genutzt wird.
Eigenschaften und Gefahren

Cyclohexan stockt bei 6,5 °C ein und siedet bei 80,7 °C. Es riecht stechend bis aromatisch-süßlich, die Geruchsschwelle liegt bei 1,4 bis 88 mg/m³, die Flüssigkeit ist leicht flüchtig. Cyclohexan bricht das Licht mit einem Brechungsindex von 1,4266. In Wasser ist Cyclohexan unlöslich, in organischen Stoffen, wie den Alkoholen, Kohlenwasserstoffen, Ethern oder Chlorkohlenwasserstoffen ist es gut löslich, Cyclohexan selbst ist ein Lösungsmittel für viele organische Stoffe. Der Flammpunkt liegt bei -26 °C, die Zündtemperatur bei 260 °C. Die Oktanzahl des Cyclohexans ist 77.
Cyclohexan ist leichtentzündlich und schwach wassergefährdend (WGK 1). Inhalation und Verschlucken der Flüssigkeit führt zu Kopfschmerzen, Übelkeit und Schwindel, die Augen und Haut rötet sie und reizt die Atemwege. Eine Langzeitexposition mit Cyclohexan kann zu Dermatitis führen.
Verwendung
Cyclohexan wird zur Produktion von Kunstfasern wie Nylon verwendet. Außerdem wird es als Lösungsmittel verwendet. Cyclohexan kommt im Erdöl vor, es ist wichtiger Ausgangsstoff für organische Synthesen. Ungefähr 39 Prozent des hergestellten Cyclohexans wird in Europa verbraucht, Europa ist der größte Abnehmer für Cyclohexan.
Herstellung
Cyclohexan wird technisch nur durch Addition von Wasserstoff an Benzol gewonnen, es kann aber auch aus dem Erdöl gewonnen werden. Die USA sind Haupthersteller von Cyclohexan, jährlich werden in den USA etwa eine Million Tonnen Cyclohexan produziert, dies entspricht etwa 34 Prozent der weltweiten Produktion. Die Gesamtproduktion des Cyclohexans in Europa beträgt jährlich zwischen 835.000 und 925.000 Tonnen.
Konformationen

Cyclohexan kann in drei Konformationen, der Sessel-, Twist- und Wannenkonformation vorliegen. Die energetisch günstigste Konformation ist die Sesselkonformation (siehe Abbildung). Es existieren zwei Sesselkonformationen, die miteinander im Gleichgewicht stehen. Beim Wechsel von der einen Sesselkonformation zur anderen werden aus axialen, das heißt senkrecht stehenden Wasserstoffatomen, äquatoriale, das heißt zur Seite stehende Wasserstoffatome und umgekehrt. Die zwei Twistkonformationen sind jeweils die Übergangsformen von den Sessel- zur Wannenkonformation und liegen energetisch zwischen Sessel- und Wannenkonformation. 99 Prozent der Cyclohexanmoleküle liegen in der Sesselkonfirmation vor, da diese energetisch am günstigsten ist, die Konformationen lassen sich aber aufgrund des nur geringen Energieunterschieds nicht voneinander isolieren.





