Mukaiyama-Hydratisierung
Die Mukaiyama-Hydratisierung ist eine organisch-chemische Reaktion, die von dem japanischen Chemiker Teruaki Mukaiyama 1989 publiziert wurde.[1]
Übersichtsreaktion
Bei der Mukaiyama-Hydratisierung wird formal ein Äquivalent Wasser an ein Alken addiert. Als Sauerstoffquelle für die entstehende Alkohol-Gruppe dient Luftsauerstoff, Wasserstoff wird vom Phenylsilan bereitgestellt. Dabei entsteht das Markownikow-Produkt. Als Katalysator für diese Reaktion dient Cobalt(II)acetylacetonat [Co(acac)2]:

Mechanismus
Der Mechanismus der Mukaiyama-Hydratisierung ist nicht vollständig geklärt. Einen ersten Mechanismus publizierte Mukaiyama 1989. Dabei nimmt er an, dass aus Alken, Cobalt-Katalysator (CoL2), Sauerstoff und dem Phenylsilan (PhSiH3) als Wasserstoffquelle ein Cobalt-Peroxid-Addukt entsteht. Durch eine Transmetallierung entsteht ein Silylperoxid. Unter Katalyse der Cobaltverbindung wird die Sauerstoff-Sauerstoff-Bindung gespalten und der Alkohol entsteht:
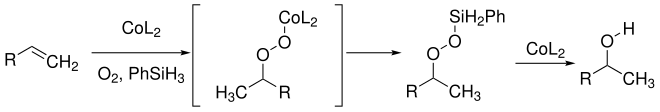
Varianten
Neben der Umsetzung von Alkenen existieren auch Protokolle zur Hydratisierung von α,β-ungesättigten Carbonylverbindungen. Sowohl die Variante nach Mukaiyama[2] als auch die von Magnus[3] nutzen einen Mangan-basierten Katalysator in dem das Acetylacetonat gegen 2,2,6,6-Tetramethyl-3,5-heptandion (Dipivaloylmethan, dmp) ausgetascht wurde. Während Mukaiyamas Arbeit sich hauptsächlich mit der Umsetzung von α,β-ungesättigten Benzylestern beschäftigt, gelingt es Magnus auch cyclische α,β-ungesättigte Ketoverbindungen zu hydratisieren:
Kritik
Die Mukaiyama-Hydratisierung zählt aus der Perspektive der Atomökonomie zu den weniger effizienten Reaktionen, da neben dem Zielmolekül (Alkohol) erhebliche Abfallmengen in mindestens stöchiometrischen Anteilen entstehen. Deshalb beschränkt sich die Anwendung auf den Labormaßstab.
Einzelnachweise
- ↑ Shigeru Isayama, Teruaki Mukaiyama: A New Method for Preparation of Alcohols from Olefins with Molecular Oxygen and Phenylsilane by the Use of Bis(acetylacetonato)cobalt(II). In: Chemistry Letters. Band 18, Nr. 6, Juni 1989, ISSN 0366-7022, S. 1071–1074, doi:10.1246/cl.1989.1071 (csj.jp [abgerufen am 11. Januar 2020]).
- ↑ Satoshi Inoki, Koji Kato, Shigeru Isayama, Teruaki Mukaiyama: A New and Facile Method for the Direct Preparation of α-Hydroxycarboxylic Acid Esters from α,β-Unsaturated Carboxylic Acid Esters with Molecular Oxygen and Phenylsilane Catalyzed by Bis(dipivaloylmethanato)manganese(II) Complex. In: Chemistry Letters. Band 19, Nr. 10, 1. Oktober 1990, ISSN 0366-7022, S. 1869–1872, doi:10.1246/cl.1990.1869 (csj.jp [abgerufen am 12. Januar 2020]).
- ↑ Philip Magnus, Andrew H Payne, Michael J Waring, David A Scott, Vince Lynch: Conversion of α,β-unsaturated ketones into α-hydroxy ketones using an MnIII catalyst, phenylsilane and dioxygen: acceleration of conjugate hydride reduction by dioxygen. In: Tetrahedron Letters. Band 41, Nr. 50, 9. Dezember 2000, ISSN 0040-4039, S. 9725–9730, doi:10.1016/S0040-4039(00)01727-5 (sciencedirect.com [abgerufen am 12. Januar 2020]).




